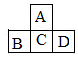题目内容
(5分)A、B、C、D四种短周期元素,原子序数D>A>B>C,且A、B同周期,C、D同主族,A的原子结构示意图为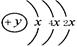 ;B、C可形成离子化合物B3C2,
;B、C可形成离子化合物B3C2,
据此利用相应的化学用语填空:
(1)A元素在周期表中的位置是 ,其气态氢化物的化学式为 。
(2)A、B、C、D四种元素的原子半径由小到大的顺序为 。
(3)B和C最高价氧化物对应水化物的化学式分别为 和 。
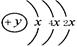 ;B、C可形成离子化合物B3C2,
;B、C可形成离子化合物B3C2,据此利用相应的化学用语填空:
(1)A元素在周期表中的位置是 ,其气态氢化物的化学式为 。
(2)A、B、C、D四种元素的原子半径由小到大的顺序为 。
(3)B和C最高价氧化物对应水化物的化学式分别为 和 。
(1)第三周期 IVA; SiH4 (2)N<P<Si<Mg (3)Mg(OH)2 HNO3
K层只能容纳2个电子,即x=2,所以A的原子序数为14,即A是硅元素。A、B同周期,即都是第三周期。又因为B、C可形成离子化合物B3C2,所以B是Mg,C是N,则D是P。同主族自上而下原子半径逐渐增大,同周期自左向右原子半径逐渐减小,所以原子半径大小顺序为N<P<Si<Mg。

练习册系列答案
 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目
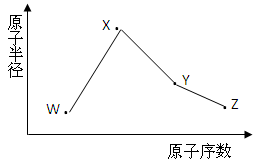
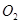 与
与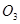
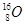 与
与