题目内容
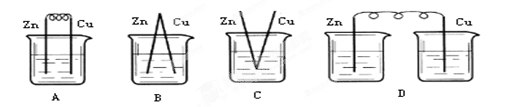
两种金属A与B和稀硫酸组成原电池时,A是正极。下列有关推断正确的是
| A.A的金属性强于B | B.电子不断由A电极经外电路流向B电极 |
| C.A电极上发生的电极反应是还原反应 | D.A的金属活动性一定排在氢前面 |
C
解析试题分析:原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。两种金属A与B和稀硫酸组成原电池时,A是正极,这说明金属性是B强于A,A不正确;电子不断由B电极经外电路流向A电极,B不正确;正极导电电子,发生还原反应,选项C正确;A的金属活动性不一定排在氢前面,选项D不正确,答案选C。
考点:考查原电池原理的应用和判断
点评:该题是基础性试题的考查,难度不大。明确原电池的工作原理是答题的关键,有利于培养学生的逻辑推理能力和发散思维能力。易错点是选项D。

练习册系列答案
相关题目
下列叙述正确的是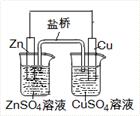
| A.电镀时,通常把待镀的金属制品作阳极 |
| B.氯碱工业是电解熔融的NaCl,在阳极能得到Cl2 |
| C.上图中电子由Zn极流向Cu,盐桥中的Cl-移向CuSO4溶液 |
| D.氢氧燃料电池(酸性电解质)中O2通入正极,电极反应为:O2+4H++4e-=2H2O |
由于具有超低耗电量、寿命长的特点,LED产品越来越受人欢迎。下图是氢氧燃料电池驱动LED发光的装置。下列有关叙述正确的是( )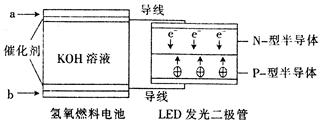
| A.a处通人氧气,b处通人氢气 |
| B.该装置中只涉及两种形式的能量转化 |
| C.电池正极电极反应式为O2+2H2O+4e-﹦4OH- |
| D.P一型半导体连接的是电池负极 |
近年,科学家们发明了一种能够给电子设备提供动力的生物燃料电池.该电池包括两个涂覆着酶的电极,它们处于充满空气和少量氢气的玻璃槽中.由于气体可以混合从而省去了昂贵的燃料隔离膜,其工作原理如图所示.下列说法正确的是 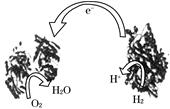
| A.左边为该电池的负极 |
| B.该电池可在高温环境下使用 |
| C.该电池负极反应为:H2-2e-=2H+ |
| D.该电池正极反应为O2+4e-=2O2- |
利用生活中常见的材料可以进行很多科学实验,甚至制作出一些有实际应用价值的装置来.下图就是一个用废旧材料制作的可用于驱动玩具的电池的示意图.该电池工作时,有关说法正确的是 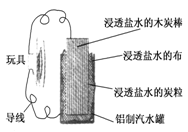
| A.炭棒应与玩具电机的负极相连 |
| B.炭粒和炭棒上发生的反应为:O2+4e-=2O2- |
| C.铝罐将逐渐被腐蚀 |
| D.该电池工作一段时间后炭棒和炭粒的质量会减轻 |
下列关于下图所示原电池装置的叙述正确的是( )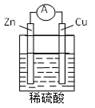
| A.铜片是负极 | B.铜片质量逐渐减少 |
| C.氢离子在铜片表面被还原 | D.电流从锌片经导线流向铜片 |