题目内容
11.价电子排布为5s25p1的元素,在周期表中的位置是( )| A. | 第4周期第VA族 | B. | 第5周期第IIIA族 | C. | 第5周期第Ⅳ族 | D. | 第4周期第IIIA族 |
分析 根据外围电子排布式可知,属于P区元素,p能级电子数不为6,为主族元素,对于主族元素,周期数等于电子层数,主族族序数等于最外层电子数.
解答 解:价电子排布为5s25p1的元素,属于P区元素,p能级电子数不为6,为主族元素,对于主族元素,周期数等于电子层数,主族族序数等于最外层电子数,故处于周期表中第五周期第ⅢA族,故选B.
点评 本题考查结构与位置关系,难度不大,注意元素周期表的结构、价电子排布与位置关系.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.黄铁矿石的主要成分为FeS2(含少量FeS,假设其他杂志中不含Fe、S元素.且高温下不发生化学变化),是我国大多数硫酸厂制取硫酸钠主要材料,某化学兴趣小组对该黄铁矿石进行如下实验探究.
将m1g该黄铁矿石的样品放入如下图装置(夹持和加热装置略)的石英管中,从a处不断地缓缓通入空气,高温灼烧黄铁矿样品至反应完全,得到红棕色固体和一种刺激性气味的气体.

【实验一】测定硫元素的含量
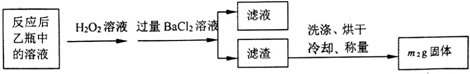
(1)甲装置的作用是除去空气中的二氧化碳,使装置乙中的溶液只吸收黄铁矿煅烧产生的二氧化硫;鼓入空气的作用是提供反应物氧气,排除装置中生成的二氧化硫,使二氧化硫完全被乙吸收.
(2)反应结束后乙瓶中的溶液需加足量H2O2溶液的目的是Na2SO3+H2O2=Na2SO4+H2O (用化学方程式表示).
(3)该黄铁矿石中硫元素的质量分数为$\frac{32{m}_{2}}{233{m}_{1}}$×100%(列出表达式即可).
【实验二】测定铁元素的含量

(4)②中,若用铁粉作还原剂,则所测得的铁元素的含量偏大 (填“偏大”、“偏小”或“无影响”).
(5)③中,需要用到的仪器除烧杯、玻璃棒、胶头滴管外,还有250mL容量瓶.
(6)④中测定时,标准KMnO4溶液应装入酸式式滴定管,滴定至终点的实验现象为:最后一滴高锰酸钾溶液滴入时,溶液颜色突变为紫色,且在30s内不变色
(7)某同学一共进行了四次滴定实验,实验结果记录如下:
根据所给数据,计算该稀释液中Fe2+的物质的量浓度为c(Fe2+)=0.500mol/L.
将m1g该黄铁矿石的样品放入如下图装置(夹持和加热装置略)的石英管中,从a处不断地缓缓通入空气,高温灼烧黄铁矿样品至反应完全,得到红棕色固体和一种刺激性气味的气体.

【实验一】测定硫元素的含量

(1)甲装置的作用是除去空气中的二氧化碳,使装置乙中的溶液只吸收黄铁矿煅烧产生的二氧化硫;鼓入空气的作用是提供反应物氧气,排除装置中生成的二氧化硫,使二氧化硫完全被乙吸收.
(2)反应结束后乙瓶中的溶液需加足量H2O2溶液的目的是Na2SO3+H2O2=Na2SO4+H2O (用化学方程式表示).
(3)该黄铁矿石中硫元素的质量分数为$\frac{32{m}_{2}}{233{m}_{1}}$×100%(列出表达式即可).
【实验二】测定铁元素的含量

(4)②中,若用铁粉作还原剂,则所测得的铁元素的含量偏大 (填“偏大”、“偏小”或“无影响”).
(5)③中,需要用到的仪器除烧杯、玻璃棒、胶头滴管外,还有250mL容量瓶.
(6)④中测定时,标准KMnO4溶液应装入酸式式滴定管,滴定至终点的实验现象为:最后一滴高锰酸钾溶液滴入时,溶液颜色突变为紫色,且在30s内不变色
(7)某同学一共进行了四次滴定实验,实验结果记录如下:
| 试验次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 消耗KmnO4溶液体积/mL | 25.00 | 25.03 | 20.00 | 24.97 |
6.原子的吸收光谱是线状的而不是连续的,主要原因是( )
| A. | 不同轨道上运动的电子具有不同的能量 | |
| B. | 外界条件的影响 | |
| C. | 仪器设备的工作原理 | |
| D. | 原子轨道的能量是量子化的 |
16.下列说法正确的是( )
| A. | 原子的原子序数越大,原子半径越大 | |
| B. | 同族元素相差的原子序数可能为16、26、36、46 | |
| C. | I A族与ⅦA族元素间可形成共价化合物或离子化合物 | |
| D. | 碱金属单质的熔点、沸点均随着原子序数的递增而升高 |
20.物质的量浓度相同的三种正盐NaX、NaY、NaZ的水溶液,其pH分别为8、9、10,则HX、HY、HZ的酸性由强到弱的顺序是( )
| A. | HX>HZ>HY | B. | HZ>HY>HZ | C. | HX>HY>HZ | D. | HY>HZ>HX |
1.用分液漏斗不能分离的混合物是( )
| A. | 水和酒精 | B. | 溴乙烷和水 | C. | 溴苯和水 | D. | 苯和水 |
 与
与
 与
与