题目内容
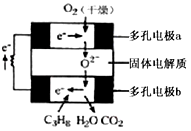
某固体燃料电池以固体氧化铝――氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池 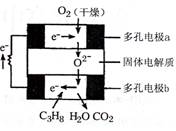 的工作原理如图所示,其中多孔电极a.b均不参与电极反应。下列判断不正确的是
的工作原理如图所示,其中多孔电极a.b均不参与电极反应。下列判断不正确的是
A.在电池内部氧离子(O2-)向负极移动
B.b极对应的电极反应式为:
C3H8+10O2-―20e-===3CO2+4H2O
C.该电池的总反应方程式为:C3H8+5O2===3CO2+4H2O
D.用该电池做点解CuSO4溶液时,每消耗1molC3H8时理论上能得到Cu的最大量为5mol
D

练习册系列答案
相关题目
 某汽车尾气分析仪以燃料电池为工作原理测定CO的浓度,其装置如图所示,该电池中电解质为氧化钇一氧化钠,其中O2-可以在固体介质NAMCON中自由移动.下列说法正确的是( )
某汽车尾气分析仪以燃料电池为工作原理测定CO的浓度,其装置如图所示,该电池中电解质为氧化钇一氧化钠,其中O2-可以在固体介质NAMCON中自由移动.下列说法正确的是( )| A、负极的电极反应式为:CO+O2--2e-?CO2 | B、工作时电子由电极b通过传感器流向电极a | C、工作时电极b作正极,02-由电极a流向电极b | D、传感器中通过的电流越大,尾气中CO的含量越低 |
 某固体燃料电池以固体氧化铝--氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过.该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应.下列判断不正确的是( )
某固体燃料电池以固体氧化铝--氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过.该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应.下列判断不正确的是( )| A、在电池内部氧离子(O2-)向负极移动 | B、b极对应的电极反应式为:C3H8+10O2--20e-═3CO2+4H2O | C、该电池的总反应方程式为:C3H8+5O2═3CO2+4H2O | D、用该电池做电解CuSO4溶液时,每消耗1mol C3H8时理论上能得到Cu的最大量为5mol |