题目内容
(共15分)
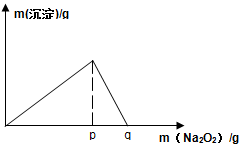
下列物质的相互转化关系中,甲、乙、丙是三种金属单质,甲燃烧时,火焰呈黄色;A、C、D为气体,C在通常情况下呈黄绿色;H为红褐色沉淀物(图中部分反应的条件和生成物未全部标出)。

(1)B的俗名: ;E的名称: 。
(2)①写出反应①的离子方程式: ;
②写出B→A的离子方程式: ;
③写出反应②的化学方程式: ;
此过程中物质的颜色变化情况为: 。
(3)①写出反应C +丙反应的化学方程式: ;
②写出反应C + F反应的离子方程式: 。
③若C+F的产物为I,则检验I中阳离子的试剂是: (化学式),现象为 。
下列物质的相互转化关系中,甲、乙、丙是三种金属单质,甲燃烧时,火焰呈黄色;A、C、D为气体,C在通常情况下呈黄绿色;H为红褐色沉淀物(图中部分反应的条件和生成物未全部标出)。

(1)B的俗名: ;E的名称: 。
(2)①写出反应①的离子方程式: ;
②写出B→A的离子方程式: ;
③写出反应②的化学方程式: ;
此过程中物质的颜色变化情况为: 。
(3)①写出反应C +丙反应的化学方程式: ;
②写出反应C + F反应的离子方程式: 。
③若C+F的产物为I,则检验I中阳离子的试剂是: (化学式),现象为 。
(1)烧碱、苛性钠、火碱(任写一个)(写氢氧化钠不给分);
盐酸(写氯化氢不给分)
(2)①2Na+2H2O=2Na++2OH-+H2↑;
②2Al+2OH-+2H2O=2AlO2-+3H2↑;
③4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(灰)白色→灰绿色→红褐色。
(3)
①2Fe+3Cl2=2FeCl3(加热或点燃)
②2Fe2++Cl2=2Fe3++2Cl-。
③KSCN,(血)红色(写到沉淀不给分)。或NaOH,红褐色沉淀
盐酸(写氯化氢不给分)
(2)①2Na+2H2O=2Na++2OH-+H2↑;
②2Al+2OH-+2H2O=2AlO2-+3H2↑;
③4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(灰)白色→灰绿色→红褐色。
(3)
①2Fe+3Cl2=2FeCl3(加热或点燃)
②2Fe2++Cl2=2Fe3++2Cl-。
③KSCN,(血)红色(写到沉淀不给分)。或NaOH,红褐色沉淀
甲为金属单质且甲燃烧时火焰呈黄色可确定甲为金属钠(Na),钠与水反应生成氢氧化钠和氢气,A为气体则A为氢气,B为氢氧化钠;C在通常情况下呈黄绿色可得到C为氯气,氢气与氯气反应生成HCl,则D为HCl气体,E为盐酸;H为红褐色沉淀物H为
Fe(OH)3进而可以得出G为Fe(OH)2,F为FeCl2,则丙单质金属为铁。
(1)B的俗名烧碱、苛性钠、火碱;E的名称为盐酸(2)①钠与水反应离子方程式为
2Na+2H2O=2Na++2OH-+H2↑;②B→A的离子方程式2Al+2OH-+2H2O=2AlO2-+3H2↑;③反应②的化学方程式4Fe(OH)2+O2+2H2O=4Fe(OH)3;该反应的现象是沉淀由白色先变为灰绿色最后变为红褐色(3)①反应C + 丙反应的化学方程式:2Fe+3Cl2=2FeCl3(加热或点燃)②反应C + F反应的离子方程式: 2Fe2++Cl2=2Fe3++2Cl-。
③C+F的产物为三氯化铁,检验Fe3+的方法是向其中加入硫氰化钾溶液,若溶液变为血红色说明原溶液中还有Fe3+
Fe(OH)3进而可以得出G为Fe(OH)2,F为FeCl2,则丙单质金属为铁。
(1)B的俗名烧碱、苛性钠、火碱;E的名称为盐酸(2)①钠与水反应离子方程式为
2Na+2H2O=2Na++2OH-+H2↑;②B→A的离子方程式2Al+2OH-+2H2O=2AlO2-+3H2↑;③反应②的化学方程式4Fe(OH)2+O2+2H2O=4Fe(OH)3;该反应的现象是沉淀由白色先变为灰绿色最后变为红褐色(3)①反应C + 丙反应的化学方程式:2Fe+3Cl2=2FeCl3(加热或点燃)②反应C + F反应的离子方程式: 2Fe2++Cl2=2Fe3++2Cl-。
③C+F的产物为三氯化铁,检验Fe3+的方法是向其中加入硫氰化钾溶液,若溶液变为血红色说明原溶液中还有Fe3+

练习册系列答案
相关题目





 896
896
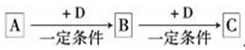
 NH4++OH-,试判断NH3溶于水后,右图中形成的NH3·H2O的合理结构是________(填序号)。
NH4++OH-,试判断NH3溶于水后,右图中形成的NH3·H2O的合理结构是________(填序号)。