题目内容
根据图示判断下列叙述符合事实的是
| A.按图①连接并放置一段时间后,Fe片表面会“镀”上一层铜 |
| B.按图②连接好导线后(Zn片与Cu片相接触),灵敏电流表会发生非常明显的偏转 |
| C.按图③连接并放置片刻,在Fe片附近加一滴KSCN溶液,溶液变为深红色 |
| D.按图④连接并放置一段时间后,在Sn片上有无色气泡聚集 |
D
解析试题分析:A、按图①连接后,铁与电源的正极相连,作阳极,铁失去电子,不可能Fe片表面会“镀”上一层铜,A不正确;B、按图②连接好导线后,由于Zn片与Cu片相接触,所以电子直接传递到铜片,因此灵敏电流表不会发生非常明显的偏转,B不正确;C、按图③连接后构成原电池,锌比铁活泼,锌是负极,铁是正极,溶液中不会产生铁离子,所以在Fe片附近加一滴KSCN溶液,溶液不可能变为深红色,C不正确;D、按图④连接后构成电解池,Sn与电源的负极相连,作阴极,溶液中的氢离子放电生成氢气,因此在Sn片上有无色气泡聚集,D正确,答案选D。
考点:考查电化学原理的有关应用与判断

用惰性电极在一定温度下电解某Na2SO4饱和溶液,当两极共产生标准状况下67.2L气体时,从溶液中析出64.4g Na2SO4?10H2O 晶体。则剩余溶液的溶质质量分数约是
| A.64.7% | B.47.5% | C.32.2% | D.28.3% |
把锌片和铁片放在盛有含酚酞的稀食盐水的玻璃器皿中,如下图。经过一段时间后,首先观察到溶液变红的区域是( )
| A.Ⅰ和Ⅲ附近 | B.Ⅰ和Ⅳ附近 |
| C.Ⅱ和Ⅲ附近 | D.Ⅱ和Ⅳ附近 |
已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd + 2NiOOH +2H2O  Cd(OH)2 + 2Ni(OH)2,有关该电池的说法正确的是( )
Cd(OH)2 + 2Ni(OH)2,有关该电池的说法正确的是( )
| A.充电过程是化学能转化为电能的过程 |
| B.充电时阳极反应:Ni(OH)2-e- + OH-=" NiOOH" + H2O |
| C.放电时负极附近溶液的碱性不变 |
| D.放电时电解质溶液中的OH-向正极移动 |
下图是氢氧燃料电池构造示意图。下列说法不正确的是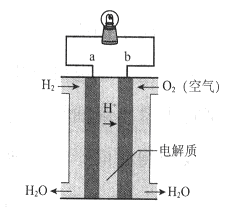
| A.a极是负极 |
| B.电子由b通过灯泡流向a |
| C.该电池总反应是2H2+ O2= 2H2O |
| D.该装置可将化学能转化为电能 |
钠硫高能蓄电池的结构如图,M为Na2O和Al2O3的混合物,电池的反应原理为 电池工作温度为320℃。下列说法错误的是
电池工作温度为320℃。下列说法错误的是
| A.a为电池正极,b为电池负极 |
B.电池放电时,正极反应为 |
| C.电池充电时.Na所在电极连接电源正极 |
| D.M的作用为导电和隔离钠和硫 |
下列化学用语的表示中,正确的是
| A.钢铁发生电化学腐蚀的负极反应式:Fe-2e-=Fe2+ |
| B.用惰性电极电解饱和食盐水时,阴极的电极反应式为:Na++e-=Na |
| C.粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e-=Cu2+ |
| D.电镀时,要在铁上镀银,则正极为银,电极反应式为:Ag+ +e-=Ag |
用石墨作电极,电解0.1 mol / L下列物质的溶液,溶液的pH值保持不变的是
| A.HCl | B.NaOH | C.Na2SO4 | D.KCl |
铅蓄电池属于二次电池。下图是铅蓄电池充、放电时的工作示意图,电解质是H2SO4溶液。电池反应为:Pb+PbO2+4H++2SO42— 2PbSO4+2H2O
2PbSO4+2H2O
下列有关说法正确的是
| A.实验室用铅蓄电池作电源电解饱和食盐水制取氯气,若制得氯气2.24L,则电池内消耗的H2SO4的物质的量是0.2mol |
| B.K与N相接时,H+向正极区迁移 |
| C.K与M连接时,所用电源的b极为负极 |
| D.K与M相接时,阳极附近的pH逐渐增大 |