题目内容
 A是化学实验室中最常见的有机物,它易溶于水并有特殊香味,并能进行如图所示的多种反应
A是化学实验室中最常见的有机物,它易溶于水并有特殊香味,并能进行如图所示的多种反应(1)写出A的结构简式:
CH3CH2OH
CH3CH2OH
(2)下列反应的化学方程式
反应①
2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
;反应③
CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O
| 浓硫酸 |
| △ |
CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O
;| 浓硫酸 |
| △ |
(3)比较反应①与钠和水反应的现象有什么相同和不同
相同点:
都有无色气泡产生,都有热量放出
都有无色气泡产生,都有热量放出
;不同点:
乙醇与钠反应时,钠沉在液面下,反应也较平稳
乙醇与钠反应时,钠沉在液面下,反应也较平稳
.分析:由图可知,A能发生与Na的取代反应,与乙酸的酯化反应,与Cu的催化氧化反应,则A为CH3CH2OH,E为乙醇钠,C为乙酸乙酯,D为乙醛,钠与水反应比钠与乙醇反应剧烈,然后结合物质的性质及化学用语来解答.
解答:解:由图可知,A能发生与Na的取代反应,与乙酸的酯化反应,与Cu的催化氧化反应,则A为CH3CH2OH,E为乙醇钠,C为乙酸乙酯,D为乙醛,
(1)由上述分析可知,A为CH3CH2OH,故答案为:CH3CH2OH;
(2)反应①为2CH3CH2OH+2Na→2CH3CH2ONa+H2↑,反应③为CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O,
故答案为:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑;CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O;
(3)因水中的羟基H比乙醇中的羟基H活泼,则反应①与钠和水的反应相比,相同点为都有无色气泡产生,都有热量放出,不同之处为乙醇与钠反应时,钠沉在液面下,反应也较平稳,故答案为:都有无色气泡产生,都有热量放出;乙醇与钠反应时,钠沉在液面下,反应也较平稳.
(1)由上述分析可知,A为CH3CH2OH,故答案为:CH3CH2OH;
(2)反应①为2CH3CH2OH+2Na→2CH3CH2ONa+H2↑,反应③为CH3COOH+CH3CH2OH
| 浓硫酸 |
| △ |
故答案为:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑;CH3COOH+CH3CH2OH
| 浓硫酸 |
| △ |
(3)因水中的羟基H比乙醇中的羟基H活泼,则反应①与钠和水的反应相比,相同点为都有无色气泡产生,都有热量放出,不同之处为乙醇与钠反应时,钠沉在液面下,反应也较平稳,故答案为:都有无色气泡产生,都有热量放出;乙醇与钠反应时,钠沉在液面下,反应也较平稳.
点评:本题考查有机物的推断,明确乙醇的性质是解答本题的关键,注意图中反应条件及物质的性质的关系即可解答,题目较简单.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案
相关题目
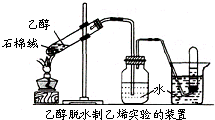 中新社2008年10月30日报道,在从日本进口的日式酱油、芥末酱中检测出了甲苯和乙酸乙酯.试回答下列问题:
中新社2008年10月30日报道,在从日本进口的日式酱油、芥末酱中检测出了甲苯和乙酸乙酯.试回答下列问题:(1)下列有关甲苯的说法不正确的是
A.甲苯和苯互为同系物
B.甲苯主要是从石油中分离获得
C.甲苯在一定条件下能发生取代、加成及氧化反应
D.为了让油漆中的甲苯等有毒物质散逸,新装璜的住房应开窗充分通风
(2)工业上常以乙醇为唯一原料一步制取乙酸乙酯,该反应的化学方程式为
(3)某学习小组拟探究实验室制乙烯,试回答下列问题.
①实验室常用乙醇在浓硫酸作用下脱水制取乙烯,该反应的化学方程式为
②上述反应以浓硫酸为催化剂,可能出现的问题有
③下表是某次探究实验现象记载.据表可知,探究实验中反应最合适的催化剂及反应温度分别是
| 催化剂 | ①浓硫酸 | ②石棉绒 (闪石) |
③P2O5 | ④浓硫酸 石棉绒 |
⑤P2O5 石棉绒 |
| KMnO4/H+褪色情况 | 褪色 | 几乎不褪色 | 褪色 | 褪色 | 褪色 |
| 加热产生气体的时间 | 45s | 50s | 35s | 47s | 38s |
| 反应温度 | 170℃ | 180℃ | 82℃ | 170℃ | 87℃ |
| 气体气流量 | 多 | 很少 | 多 | 较多 | 较多 |
| 反应液炭化情况 | 严重 | 无炭化 | 无炭化 | 严重 | 无炭化 |
(15分)中新社2008年10月30日报道,在从日本进口的日式酱油、芥末酱中检测出了甲苯和乙酸乙酯。试回答下列问题:
(1)下列有关甲苯的说法不正确的是 ▲ (填写选项字母)。
A.甲苯和苯互为同系物
B.甲苯主要是从石油中分离获得
C.甲苯在一定条件下能发生取代、加成及氧化反应
D.为了让油漆中的甲苯等有毒物质散逸,新装璜的住房应开窗充分通风
(2)工业上常以乙醇为唯一原料一步制取乙酸乙酯,该反应的化学方程式为 ▲ 。
 (3)某学习小组拟探究实验室制乙烯,试回答下列问题。
(3)某学习小组拟探究实验室制乙烯,试回答下列问题。
①实验室常用乙醇在浓硫酸作用下脱水制取乙烯,该反应的化学方程式为 ▲ 。
②上述反应以浓硫酸为催化剂,可能出现的问题有 ▲ 、 ▲ 等。
③下表是某次探究实验现象记载。据表可知,探究实验中反应最合适的催化剂及反应温度分别是 ▲ 、 ▲ 。
| 催化剂 | ①浓硫酸 | ②石棉绒 (闪石) | ③P2O5 | ④浓硫酸 石棉绒 | ⑤P2O5 石棉绒 |
| KMnO4/H+褪色情况 | 褪色 | 几乎不褪色 | 褪色 | 褪色 | 褪色 |
| 加热产生气体的时间 | 45s | 50s | 35s | 47s | 38s |
| 反应温度 | 170℃ | 180℃ | 82℃ | 170℃ | 87℃ |
| 气体气流量 | 多 | 很少 | 多 | 较多 | 较多 |
| 反应液炭化情况 | 严重 | 无炭化 | 无炭化 | 严重 | 无炭化 |
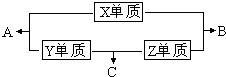 X、Y、Z、M三种短周期元素,其中X、Y、Z的原子序数之和为16,X、Y、Z三种元素的常见单质在常温常压下都是无色气体,在适当的条件下可以发生如下图所示的变化:
X、Y、Z、M三种短周期元素,其中X、Y、Z的原子序数之和为16,X、Y、Z三种元素的常见单质在常温常压下都是无色气体,在适当的条件下可以发生如下图所示的变化:
 X、Y、Z、M三种短周期元素,其中X、Y、Z的原子序数之和为16,X、Y、Z三种元素的常见单质在常温常压下都是无色气体,在适当的条件下可以发生如下图所示的变化:
X、Y、Z、M三种短周期元素,其中X、Y、Z的原子序数之和为16,X、Y、Z三种元素的常见单质在常温常压下都是无色气体,在适当的条件下可以发生如下图所示的变化: