题目内容
不同元素的原子在分子内吸引电子能力的强弱可用一定数值x(电负性)来表示,若x越大,其原子吸引电子的能力越强,在所形成的分子中成为负电荷一方。下面是某些短周期元素的x值: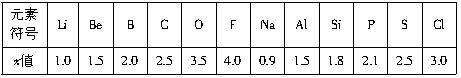
(1)通过分析x值的变化规律,确定N、Mg的x值范围:_________<x(Mg)<_________,________<x(N)<__________。
(2)推测x值与原子半径的关系是______________
___________________________;短周期元素的x值的变化特点体现了元素性质的___________变化规律。
(3)某有机物的结构式为
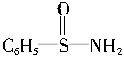 ,其中S―N中,你认为共用电子对偏向谁?__________(写原子名称)。
,其中S―N中,你认为共用电子对偏向谁?__________(写原子名称)。(4)经验规律告诉我们当成键的两原子相应元素的x的差值△x>1.7 时,一般为离子键,当△x<1.7时,一般为共价键,试推断AlBr3中化学键的类型是____________。
(5)预测元素周期表中,x值最小的元素的位置:_______________________(放射性元素除外)。
(1)0.9;1.5;2.5;3.5
(2)同周期(同主族)中,x值越大,其原子半径越小;周期性
(3)氮原子
(4)共价键
(5)第6周期ⅠA族
【试题分析】

练习册系列答案
相关题目

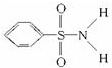 ,其中S-N中,你认为共用电子对偏向
,其中S-N中,你认为共用电子对偏向