题目内容
将3.25 g某金属跟过量稀硝酸反应时,未观察到有气体放出,但测知生成物中有NH4NO3。当向反应后的溶液中加入过量热的烧碱溶液时,可放出一种气体,体积为280 mL(标准状况)。
(1)如金属以M表示,试写出有关的化学方程式。
(2)试推断M是哪种金属。(必须写出推断过程)
解析:
nNH4NO3+nNaOH nH2O+nNH3↑+nNaNO3 (2)锌
|
提示:
设金属M的硝酸盐为M(NO3)n,依题意,写出反应方程式,并计算讨论得知M为何金属。
nNH4NO3+nNaOH nH2O+nNH3↑+nNaNO3 (2)设金属的原子量为x,化合价为+n,根据题意n(NH
可得 x=32.5 n(n可为1、2、3、4) 当 n=1时,x=32.5,无对应金属元素。 n=2,x=65,锌。 n=3或4,均无对应金属元素。 故M为锌。
|

 阅读快车系列答案
阅读快车系列答案(共12分)随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视。
Ⅰ.目前工业上有一种方法是用CO2来生产燃料甲醇。为探究该反应原理,进行如下实验,在体积为1L的密闭容器中,充入1mol CO2和3.25 mol H2,在一定条件下发生反应,测定CO2、CH3OH(g)和H2O(g)的浓度随时间变化如下图所示: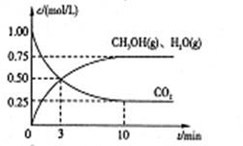
(1)从反应开始到平衡,氢气的平均反应速率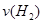 = mol/(L·min)
= mol/(L·min)
(2)该条件下CO2的转化率为 。
(3)下列措施中能使n(CH3OH)/n(CO2)增大的是 。
| A.升高温度 | B.恒容时充入氮气 |
| C.将水蒸气从体系中分离 | D.用更有效的催化剂 |
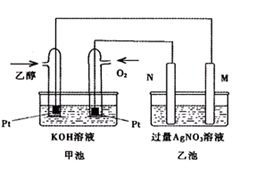
(1)M极的电极材料为 。
(2)加入乙醇的铂电极的电极反应式为 。
(3)在此过程中乙池中某一电极析出金属银4.32g时,此时乙池溶液的体积为400mL,则乙池中溶液的pH为 。
(4)若在常温常压下,1g C2H5OH燃烧生成CO2和液态H2O时放出29.71kJ热量,表示该反应的热化学方程式为 。