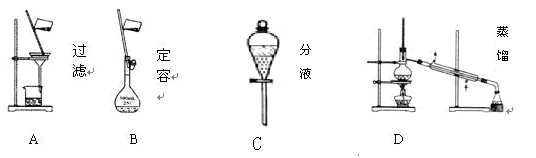
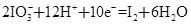��Ŀ����
�о�̼���仯������ۺ����öԴٽ���̼���Ĺ���������Ҫ�����塣���������֪ʶ�о�̼���仯��������ʡ�
��1�����������ҹ��õ绡���ϳɵ�̼�����г����д���̼�����������ʣ�������̼���������������������ᴿ���䷴Ӧ�Ļ�ѧ����ʽΪ��
C+ K2Cr2O7+ �� CO2��+ K2SO4 + Cr2(SO4)3+ H2O
����ɲ���ƽ������ѧ����ʽ��
������������ʽ���õ����ű���÷�Ӧ����ת�Ƶķ�������Ŀ��
��2������ʱ����CO��ԭMgSO4���Ʊ��ߴ�MgO��
��750��ʱ����������к������ʵ���SO2��SO3����ʱ��Ӧ�Ļ�ѧ����ʽ�� ��
����MgO���Ƴɡ�þ���������Ρ���أ���װ��ʾ��ͼ��ͼ1���õ�ط�Ӧ�����ӷ���ʽΪ �� 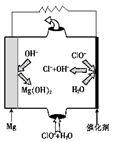
 ��
�� 
ͼ1 ͼ2 ͼ3
��3��������̼�ϳɼ״���̼���ŵ��·���CO2ת��Ϊ�״����Ȼ�ѧ����ʽΪ��CO2(g) +3H2(g) CH3OH(g) +H2O(g) ��H
CH3OH(g) +H2O(g) ��H
�ٸ÷�Ӧ��ƽ�ⳣ������ʽΪK�� ��
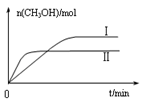
��ȡ��ݵ����CO2��H2�Ļ������(���ʵ���֮�Ⱦ�Ϊ1��3)���ֱ�����¶Ȳ�ͬ���ݻ���ͬ�ĺ����ܱ������У�����������Ӧ����Ӧ��ͬʱ���ü״������������(CH3OH)�뷴Ӧ�¶�T�Ĺ�ϵ������ͼ2��ʾ��������CO2ת��Ϊ�״���Ӧ�ġ�H 0(�>����<������)��
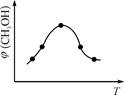
�������ֲ�ͬ�����·�����Ӧ�����CH3OH�����ʵ�����ʱ��仯��ͼ3��ʾ������I��II��Ӧ��ƽ�ⳣ����С��ϵΪK�� KII(����� ����������)��
��1����3 2 8 H2SO4 3 2 2 8 ��2�֣�
��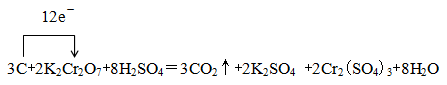 ��1�֣�
��1�֣�
��2����2MgSO4 + CO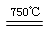 2MgO + SO2 + CO2 + SO3��3�֣�
2MgO + SO2 + CO2 + SO3��3�֣�
��Mg + ClO- + H2O��Cl- + Mg(OH)2��3�֣�
��3����K�� ��2�֣� �ڣ� ��2�֣� �ۣ� ��2�֣�
��2�֣� �ڣ� ��2�֣� �ۣ� ��2�֣�
���������������1���ٸ��ݷ�Ӧʽ��֪����Ӧ��̼Ԫ�صĻ��ϼ۴�0�����ߵ���4�ۣ�ʧȥ4�����ӣ�̼�ǻ�ԭ����CrԪ�صĻ��ϼ۴ӣ�6�۽��͵���3�ۣ��õ�3�����ӣ�K2Cr2O7�������������ݵ��ӵ�ʧ�غ��֪����ԭ��̼��������K2Cr2O7�����ʵ���֮����3:2������ԭ���غ��֪����Ӧǰ��������μӣ������ƽ��ķ���ʽΪ3C+2K2Cr2O7+8H2SO4��3CO2��+2K2SO4 +2Cr2(SO4)3+8H2O��
�ڸ��ݢٿ�֪���õ����ű���÷�Ӧ����ת�Ƶķ�������ĿΪ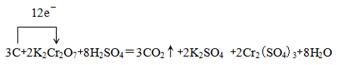 ��
��
��2������CO��ԭMgSO4����750��ʱ����������к������ʵ���SO2��SO3������SԪ�صĻ��ϼ۴ӣ�6�۽��͵���4�ۣ��õ�2�����ӣ����Ը��ݵ��ӵ�ʧ�غ��֪��CO������������CO2������SO2�����ʵ�����ȣ���˴�ʱ��Ӧ�Ļ�ѧ����ʽ��2MgSO4 + CO 2MgO + SO2 + CO2 + SO3��
2MgO + SO2 + CO2 + SO3��
�ڸ���ͼ1��֪��þ�Ǹ���ʧȥ����ת��Ϊ������þ�����������������õ����ӣ�����ԭΪ�����ӣ����Ըõ�ص��ܷ�Ӧ���ӷ���ʽΪMg + ClO- + H2O��Cl- + Mg(OH)2��
��3���ٻ�ѧƽ�ⳣ������һ�������£������淴Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ�����Ը��ݷ���ʽ��֪�÷�Ӧ��ƽ�ⳣ������ʽΪK�� ��
��
�ڸ���ͼ2��֪���ڼ״��ĺ����ﵽ���ֵ����������¶ȣ��״��ĺ����������ͣ���˵�������¶�ƽ�����淴Ӧ�����ƶ����������Ӧ�Ƿ��ȷ�Ӧ������H��0��
�۸���ͼ3��֪�����ߢ����ȴﵽƽ��״̬����˵�����ߢ�ķ�Ӧ���ʿ졣�����ߢ��Ӧ�ļ״����ʵ���С������I��Ӧ�ļ״������ʵ��������ڸ÷�Ӧ�������С�ķ��ȵĿ��淴Ӧ�����Է�Ӧ����Ӧ���������¶ȣ���ʹƽ�����淴Ӧ�����ƶ������ƽ�ⳣ����С����K����KII��
���㣺����������ԭ��Ӧ��ƽ����ʾ��ԭ����жϣ�ƽ�ⳣ���Լ����������ƽ��״̬��Ӱ��

�о�NO2��SO2��CO�ȴ�����Ⱦ����Ĵ���������Ҫ���塣
��1�����÷�Ӧ��6NO2��8NH3 7N2��12H2O�ɴ���NO2����ת��1.2mol����ʱ�����ĵ�NO2�ڱ�״���µ������ L��
7N2��12H2O�ɴ���NO2����ת��1.2mol����ʱ�����ĵ�NO2�ڱ�״���µ������ L��
��2������֪��2SO2(g)+O2(g) 2SO3(g) ��H��?196.6 kJ��mol�C1
2SO3(g) ��H��?196.6 kJ��mol�C1
2NO(g)+O2(g) 2NO2(g) ��H��?113.0 kJ��mol�C1
2NO2(g) ��H��?113.0 kJ��mol�C1
��д��NO2��SO2��Ӧ����SO3(g)��NO���Ȼ�ѧ����ʽ ��
��һ�������£���NO2��SO2�������1:2�����ܱ������з���������Ӧ��������˵����Ӧ�ﵽƽ��״̬���� ��
a����ϵѹǿ���ֲ��� b�����������ɫ���ֲ���
c��SO3��NO������ȱ��ֲ��� d��ÿ����1 mol SO2��ͬʱ����1 molNO2
�۲��������Ӧƽ��ʱNO2��SO2�����Ϊ1:6����÷�Ӧ��ƽ�ⳣ��K�� ��
��3������β���е�һ����̼��ͨ�����·�Ӧ������Ũ�ȣ�CO(g)+1/2O2(g) CO2(g)����֪ij�¶��£������������ܱ������н��и÷�Ӧ�������и����ʵ���ʼŨ�ȼ������淴Ӧ���ʹ�ϵ���±���ʾ�����á���������������д���еĿո�
CO2(g)����֪ij�¶��£������������ܱ������н��и÷�Ӧ�������и����ʵ���ʼŨ�ȼ������淴Ӧ���ʹ�ϵ���±���ʾ�����á���������������д���еĿո�
| ������� | c(CO)��mol��L�C1 | c(O2)��mol��L�C1 | c(CO2)��mol��L�C1 | ��(��)�ͦ�(��) ��С�Ƚ� |
| �� | 2.0��10�C4 | 4.0��10�C4 | 4.0��10�C4 | ��(��)����(��) |
| �� | 1.0��10�C3 | 4.0��10�C4 | 5.0��10�C4 | ��(��) ��(��) |
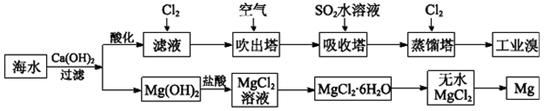
������������Դ�������ȷ������Ź㷺����;��ʪ�����ɷ��Ʊ��������ε�ԭ�����±���ʾ��
��1����ҵ����ʪ���Ʊ�������أ�K2FeO4������������ͼ��ʾ��
|
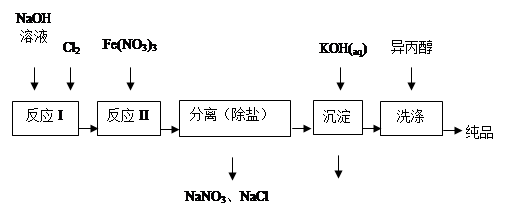 ��ϴ�Ӵ�Ʒʱѡ�������������ˮ�������ǣ� ��
��ϴ�Ӵ�Ʒʱѡ�������������ˮ�������ǣ� ���ڷ�ӦI�Ļ�ѧ����ʽΪ ��
�۷�ӦII�����ӷ���ʽΪ ��
����֪25��ʱFe(OH)3��Ksp = 4.0��10-38����ӦII�����Һ��c(Fe3+)=4.0��10-5 mol/L,����Ҫ����pH= ʱ����ʼ����Fe(OH)3����������Һ����ı仯����
��2��������ͼ�ɼ���ʪ���Ʊ��������ʱ�������Ƶø������ƣ�Ȼ��������������м��뱥��KOH��Һ����������������ء�
�ټ��뱥��KOH��Һ��Ŀ���ǣ� ��
����������Ϣ��֪��������ص��ܽ�ȱȸ������� �����С������
| ʪ�� | ǿ���Խ����У�Fe(NO3)3��NaClO��Ӧ�����Ϻ�ɫ����������Һ |
| �ɷ� | Fe2O3��KNO3��KOH��ϼ��ȹ��������Ϻ�ɫ�������κ�KNO2�Ȳ��� |
��3���ɷ��Ʊ�K2FeO4�ķ�Ӧ���������뻹ԭ�������ʵ���֮��Ϊ ��
 6Cu��SO2�����÷�Ӧ����������______________��������19.2 g Cuʱ����Ӧ��ת�Ƶĵ���Ϊ__________mol��
6Cu��SO2�����÷�Ӧ����������______________��������19.2 g Cuʱ����Ӧ��ת�Ƶĵ���Ϊ__________mol��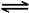 CO2(g)��H2(g) ��H����41kJ/mol��ij�¶��£����ݻ�Ϊ2L���ܱ������г���2.0molCO(g)��2.0molH2O(g)����tminʱ�ﵽƽ�⣬��÷ų���32.8kJ��������tmin����H2��ʾ��ƽ����Ӧ����Ϊ ���ɴ˿�֪�ڸ��¶��·�ӦCO2(g)��H2(g)
CO2(g)��H2(g) ��H����41kJ/mol��ij�¶��£����ݻ�Ϊ2L���ܱ������г���2.0molCO(g)��2.0molH2O(g)����tminʱ�ﵽƽ�⣬��÷ų���32.8kJ��������tmin����H2��ʾ��ƽ����Ӧ����Ϊ ���ɴ˿�֪�ڸ��¶��·�ӦCO2(g)��H2(g)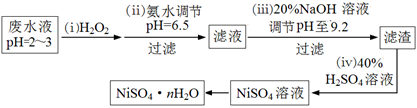
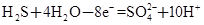 ��
��