题目内容
3.已知:C(s)+$\frac{1}{2}$O2(g)═CO(g);△H1=-110.35kJ•mol-1CO(g)+$\frac{1}{2}$O2(g)═CO2(g);△H2=-282.57kJ•mol-1
则C(s)+O2(g)═CO2(g);△H3为( )
| A. | +172.22 kJ•mol-1 | B. | -172.22 kJ•mol-1 | ||
| C. | +392.92 kJ•mol-1 | D. | -392.92 kJ•mol-1 |
分析 根据盖斯定律构造出目标反应热化学反应方程式,据此计算反应热;注意化学计量数乘以不同的系数,进行加减,焓变也要乘以相同的系数,做相应加减.
解答 解:①C(s)+$\frac{1}{2}$O2(g)=CO(g)△H1=-110.35kJ/mol,②CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H2=-282.57kJ/mol,根据盖斯定律,①+②得:C(s)+O2(g)=CO2(g),△H=-110.35kJ/mol+(-282.57kJ/mol)=-392.92kJ/mol,
故选D.
点评 本题考查了盖斯定律的计算应用,注意热化学方程式系数变化焓变随之变化,反应改变方向,焓变改变符号,题目较简单.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14. 某探究小组用HNO3与大理石反应过程中质量减小的方法研究影响反应速率的因素.所用HNO3浓度为1.00mol•L-1、2.00mol•L-1,大理石有细颗粒与粗颗粒两种规格,实验温度为298K、308K,每次实验HNO3用量为25.0mL,大理石用量为10.00g.
某探究小组用HNO3与大理石反应过程中质量减小的方法研究影响反应速率的因素.所用HNO3浓度为1.00mol•L-1、2.00mol•L-1,大理石有细颗粒与粗颗粒两种规格,实验温度为298K、308K,每次实验HNO3用量为25.0mL,大理石用量为10.00g.
(1)请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
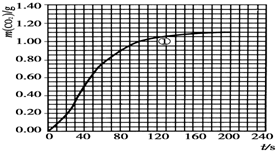
(2)实验①中CO2质量随时间变化的关系见图:
依据反应方程式$\frac{1}{2}$CaCO3+HNO3═$\frac{1}{2}$Ca(NO3)2+$\frac{1}{2}$CO2↑+$\frac{1}{2}$H2O,计算实验①在70~90s范围内HNO3的反应速率(忽略溶液体积变化,写出计算过程).
 某探究小组用HNO3与大理石反应过程中质量减小的方法研究影响反应速率的因素.所用HNO3浓度为1.00mol•L-1、2.00mol•L-1,大理石有细颗粒与粗颗粒两种规格,实验温度为298K、308K,每次实验HNO3用量为25.0mL,大理石用量为10.00g.
某探究小组用HNO3与大理石反应过程中质量减小的方法研究影响反应速率的因素.所用HNO3浓度为1.00mol•L-1、2.00mol•L-1,大理石有细颗粒与粗颗粒两种规格,实验温度为298K、308K,每次实验HNO3用量为25.0mL,大理石用量为10.00g.(1)请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
| 实验编号 | T/K | 大理石规格 | HNO3浓度/mol•L-1 | 实验目的 |
| ① | 298 | 粗颗粒 | 2.00 | (Ⅰ)实验①和②探究HNO3的浓度对该反应速率的影响; (Ⅱ)实验①和③探究温度对该反应速率的影响; (Ⅲ)实验①和④探究大理石规格 (粗、细)对该反应速率 的影响. |
| ② | ||||
| ③ | ||||
| ④ |
依据反应方程式$\frac{1}{2}$CaCO3+HNO3═$\frac{1}{2}$Ca(NO3)2+$\frac{1}{2}$CO2↑+$\frac{1}{2}$H2O,计算实验①在70~90s范围内HNO3的反应速率(忽略溶液体积变化,写出计算过程).
18.已知某含苯环的分子C8H10,苯环上有两个侧链,其一氯取代物的种数是(不考虑立体异构)( )
| A. | 10种 | B. | 9种 | C. | 6种 | D. | 5种 |
8.下列实验能获得成功的是( )
| A. | 在某淀粉溶液中加入适量的稀硫酸,并加热一段时间,待冷却后,再加入银氨溶液来检验淀粉是否已发生水解 | |
| B. | 把R-X与NaOH水溶液混合,加入硝酸银溶液来验证R-X是否为碘代烷 | |
| C. | 在三颈烧瓶中先加入少量铁粉,再加入5mL苯和1mL液溴的混合物,待充分反应后可制得少量溴苯 | |
| D. | 将无水乙醇和浓硫酸共热至140℃可制得乙烯 |
15.可逆反应2SO2+O2?2SO3达到平衡的标志是( )
①消耗2mol SO2的同时生成2mol SO3
②SO2、O2与SO3的物质的量之比为2:1:2
③反应混合物中,SO3的质量分数不再改变.
①消耗2mol SO2的同时生成2mol SO3
②SO2、O2与SO3的物质的量之比为2:1:2
③反应混合物中,SO3的质量分数不再改变.
| A. | ①② | B. | ①③ | C. | 只有③ | D. | 全部 |
12.甲、乙两烧杯分别装有100mL相同pH的氨水和氢氧化钠溶液,向其中各加入10mL 0.1mol/L AlCl3溶液,两烧杯中都有沉淀生成,下列判断错误的是( )
| A. | 两烧杯中的沉淀可能一样多 | |
| B. | 两烧杯中沉淀的最大可能值均为0.078g | |
| C. | 反应后两烧杯中溶液的pH可能:甲<乙 | |
| D. | 两烧杯中反应的离子方程式不同 |
1.某有机物的结构简式为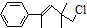 ,下列关于该有机物的叙述不正确的是( )
,下列关于该有机物的叙述不正确的是( )
 ,下列关于该有机物的叙述不正确的是( )
,下列关于该有机物的叙述不正确的是( )| A. | 能使酸性KMnO4溶液褪色 | B. | 能使溴水褪色 | ||
| C. | 在一定条件下可以发生加聚反应 | D. | 一定条件下,能和NaOH醇溶液反应 |
