题目内容
生物质能是一种洁净、可再生能源。生物质气(主要成分为CO、CO2、H2等)与混合,在含有Zn、Cu等元素的催化剂条件下能合成一种生物质能——甲醇。
(1) 与CO互为等电子体的物质的化学式是 。
(2) CO2分子中碳原子的杂化类型是 杂化。
(3) 按电子排布Zn在元素周期表中属于 区,
其晶体属于六方最密堆积,它的配位数是 。
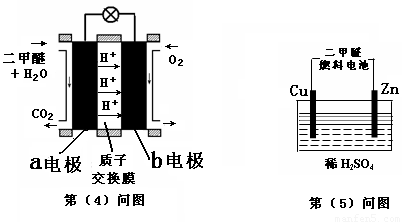
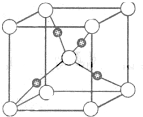
(4) Cu的一种氯化物晶体的晶胞结构如图所示。(空心球代表氯离子),则一个晶胞中所含的数目是 。
【答案】
(1)N2(2)sp(3)ds 12(4)4
【解析】
试题分析: (1)等电子体原子数相同、价电子数相同。与CO互为等电子体的分子是N2。
(2)CO2分子中C价层电子对数= 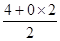 =2,C杂化类型为sp。
=2,C杂化类型为sp。
(3)锌位于IIB族,属于ds区元素。六方最密堆积配位数为12。
(4)晶胞中绿球和蓝球个数分别为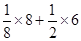 =4、8。
=4、8。
考点: 等电子体 中心原子杂化类型 元素周期表的分区 金属晶体堆积模型 晶胞计算

练习册系列答案
相关题目
 生物质能是一种洁净、可再生的能源.生物质气(主要成分为CO、CO2、H2等)与H2混合,催化合成甲醇是生物质能利用的方法之一.
生物质能是一种洁净、可再生的能源.生物质气(主要成分为CO、CO2、H2等)与H2混合,催化合成甲醇是生物质能利用的方法之一.
 CO2(g)+H2(g),该反应的△H________0(选填:“>”、“<”、“=”);在900K时,该反应平衡常数的对数值(lgK)=_____________.
CO2(g)+H2(g),该反应的△H________0(选填:“>”、“<”、“=”);在900K时,该反应平衡常数的对数值(lgK)=_____________.