题目内容
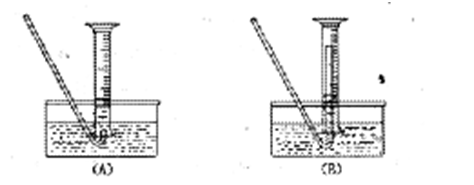
(11分)右图表示在没有通风橱的条件下制备氯气时设计的装置, 图中a、b是可控制的弹簧铁夹。(氯气在饱和氯化钠溶液中的溶解度较小。)
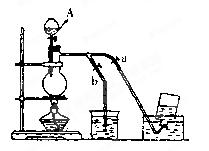
⑴仪器A的名称是 ;水槽中应盛放的 是 ;烧杯中盛放的是 ;
;
烧瓶中反应的化学方程式 ;
⑵当收集氯气时打开 ,关闭___ 。当氯气收集完毕时打开 ,
关闭___ 。(填a,b)烧杯中反应的化学方程式 。

⑴仪器A的名称是 ;水槽中应盛放的 是 ;烧杯中盛放的是
 ;
;烧瓶中反应的化学方程式 ;
⑵当收集氯气时打开 ,关闭___ 。当氯气收集完毕时打开 ,
关闭___ 。(填a,b)烧杯中反应的化学方程式 。
(11分)(方程式2分,余1分)
⑴分液漏斗;饱和食盐水;氢氧化钠溶液 ;
 MnO2+4HCl(浓)
MnO2+4HCl(浓)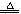 MnCl2+Cl2 +2H2O;(条件、符号不扣分)
MnCl2+Cl2 +2H2O;(条件、符号不扣分)⑵ a ,__b ; b ,__a ;Cl2+2NaOH==NaCl+NaClO+H2O。
略

练习册系列答案
相关题目

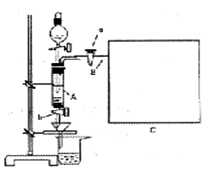

 MnCl2+2H2O+ Cl2↑
MnCl2+2H2O+ Cl2↑ +4)制取纳米级TiO2的流程如下:
+4)制取纳米级TiO2的流程如下: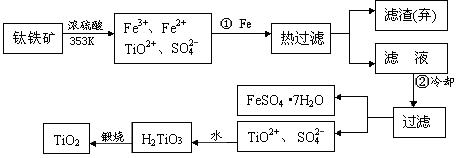
 TiCl4
TiCl4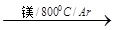 Ti
Ti 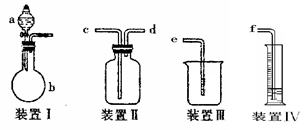
 置序号
置序号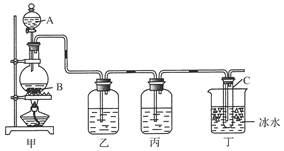
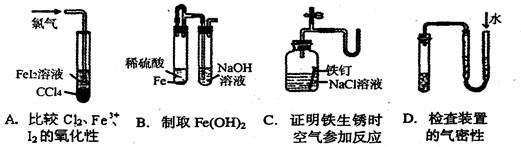
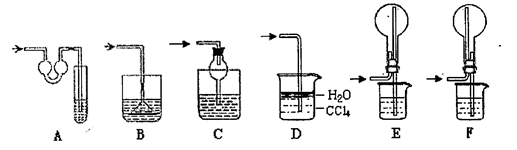
 实验目的的是( )
实验目的的是( )