题目内容
在一定条件下,对于密闭容器中进行的可逆反应A(g)+3B(g)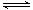
|
A.A、B、C的分子数之比为1∶3∶2
B.A、B、C的浓度相等
C.单位时间生成 n mol A,同时生成 3n mol B
D.生成C的速率与C分解的速率相等
【答案】
D
【解析】
试题分析:在一定条件下,当可逆反应中正反应速率和逆反应速率相等时(但不为0),各种物质的浓度或含量均不再发生变化的状态,是化学平衡状态,据此可以判断。平衡时浓度不再发生变化,但物质之间的浓度不一定相等或满足某种关系,因此A和B都是不正确的;物质A和B都是反应物,且二者的化学计量数之比是1:3,因此单位时间生成 n mol A,一定同时生成 3n mol B,所以不能说明反应达到平衡状态,C不正确;生成C的速率与C分解的速率相等,即正逆反应速率相等,说明反应达到平衡状态,D正确,答案选D。
考点:考查可逆反应平衡状态的判断

练习册系列答案
相关题目
在一定条件下,对于密闭容器中进行的可逆反应:N2(g)+3H2(g)
2NH3(g)下列说法中,能充分说明这一反应已经达到化学平衡状态的是( )
| 催化剂 |
| △ |
| A、N2、H2与NH3的物质的量之比为1:3:2 |
| B、N2、H2与NH3的浓度相等 |
| C、正、逆反应速率相等且不等于零 |
| D、反应停止,正、逆反应速率都等于零 |
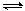
 2C(g),下列说法中,能说明这一反应已经达到化学平衡状态的是( )
2C(g),下列说法中,能说明这一反应已经达到化学平衡状态的是( ) 2SO3(g).下列说法中,表明这一反应已经达到化学平衡状态的是( )
2SO3(g).下列说法中,表明这一反应已经达到化学平衡状态的是( )