题目内容
能正确表示CH4中碳原子的成键轨道的示意图为( )


D
试题分析:甲烷是正四面体型结构,其中碳原子是sp3杂化,所以碳原子的成键轨道的示意图为
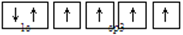 ,答案选D。
,答案选D。点评:该题设计新颖,基础性强,侧重对学生能力的培养。该题的关键是明确甲烷分子中碳原子的杂化轨道类型,然后灵活运用即可,有利于调动学生的学习积极性,提高学生的应试能力。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
题目内容

 ,答案选D。
,答案选D。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案