籾朕坪否
械梁和⇧泌惚函0.1 mol,L⇩1 HA卑匣嚥0.1 mol,L⇩1 NaOH卑匣吉悶持詞栽(策待詞栽朔卑匣悶持議延晒)⇧霞誼詞栽卑匣議pH﹆8⇧編指基參和諒籾⦿
(1)詞栽卑匣議pH﹆8議圻咀(喘宣徨圭殻塀燕幣)⦿ 。
(2)詞栽卑匣嶄喇邦窮宣竃議c(OH⇩) (野^﹅ ̄、^〽 ̄賜^﹆ ̄)0.1 mol,L⇩1 NaOH卑匣嶄喇邦窮宣竃議c(OH⇩)。
(3)箔竃詞栽卑匣嶄和双麻塀議娼鳩柴麻潤惚(野醤悶方忖)⦿c(Na⇦)⇩c(A⇩)﹆ mol,L⇩1⇧c(OH⇩)⇩c(HA)﹆ mol,L⇩1。
(4)厮岑NH4A卑匣葎嶄來⇧嗽岑HA卑匣紗欺Na2CO3卑匣嶄嗤賑悶慧竃⇧編容僅(NH4)2CO3卑匣議pH 7(野^﹅ ̄、^〽 ̄賜^﹆ ̄)◉繍揖梁業和吉敵業議膨嶽冦卑匣⦿
A⤴NH4HCO3 B⤴NH4A C⤴(NH4)2SO4 D⤴NH4Cl
梓pH喇寄欺弌議乏會電双頁 (野會催)。
(1)詞栽卑匣議pH﹆8議圻咀(喘宣徨圭殻塀燕幣)⦿ 。
(2)詞栽卑匣嶄喇邦窮宣竃議c(OH⇩) (野^﹅ ̄、^〽 ̄賜^﹆ ̄)0.1 mol,L⇩1 NaOH卑匣嶄喇邦窮宣竃議c(OH⇩)。
(3)箔竃詞栽卑匣嶄和双麻塀議娼鳩柴麻潤惚(野醤悶方忖)⦿c(Na⇦)⇩c(A⇩)﹆ mol,L⇩1⇧c(OH⇩)⇩c(HA)﹆ mol,L⇩1。
(4)厮岑NH4A卑匣葎嶄來⇧嗽岑HA卑匣紗欺Na2CO3卑匣嶄嗤賑悶慧竃⇧編容僅(NH4)2CO3卑匣議pH 7(野^﹅ ̄、^〽 ̄賜^﹆ ̄)◉繍揖梁業和吉敵業議膨嶽冦卑匣⦿
A⤴NH4HCO3 B⤴NH4A C⤴(NH4)2SO4 D⤴NH4Cl
梓pH喇寄欺弌議乏會電双頁 (野會催)。
(1)A⇩⇦H2O HA⇦OH⇩
HA⇦OH⇩
(2)﹅
(3)9.9〜10⇩7 10⇩8
(4)﹅ A﹅B﹅D﹅C
 HA⇦OH⇩
HA⇦OH⇩(2)﹅
(3)9.9〜10⇩7 10⇩8
(4)﹅ A﹅B﹅D﹅C
(2)詞栽卑匣喇噐A⇩邦盾⇧陥序邦議窮宣⇧遇NaOH雙崙邦議窮宣。
(3)匯蝕兵c(Na⇦)﹆c(A⇩)⇧徽Na⇦音邦盾⇧A⇩邦盾⇧c(Na⇦)嚥c(A⇩)岻餓軸葎邦盾議A⇩議楚。pH﹆8⇧c(H⇦)﹆10⇩8 mol,L⇩1⇧c(OH⇩)﹆10⇩6 mol,L⇩1。
喇H2O窮宣議c(OH⇩)H2O﹆c(H⇦)﹆10⇩8 mol,L⇩1
A⇩⇦H2O HA⇦OH⇩
HA⇦OH⇩
夸c(Na⇦)⇩c(A⇩)﹆c(OH⇩)⇩c(OH⇩)H2O﹆9.9〜10⇩7 mol,L⇩1
c(OH⇩)⇩c(HA)﹆10⇩6 mol,L⇩1⇩9.9〜10⇩7 mol,L⇩1﹆10⇩8 mol,L⇩1
(4)NH4A卑匣葎嶄來⇧傍苧NH4+嚥A⇩議邦盾殻業屢輝⇧遇HA紗欺Na2CO3嶄嗤賑悶慧竃⇧傍苧HA磨來膿噐H2CO3⇧CO32-邦盾殻業寄噐A⇩⇧咀遇(NH4)2CO3卑匣pH﹅7⇧NH4HCO3卑匣議pH匆揖劔寄噐7。Cl⇩才SO42-音邦盾⇧侭參(NH4)2SO4才NH4Cl卑匣𠮟磨來⇧徽(NH4)2SO4嶄NH4+厚謹⇧邦盾殻業厚寄⇧咀遇pH[(NH4)2SO4]〽pH(NH4Cl)〽7﹆pH(NH4A)〽pH(NH4HCO3)。
(3)匯蝕兵c(Na⇦)﹆c(A⇩)⇧徽Na⇦音邦盾⇧A⇩邦盾⇧c(Na⇦)嚥c(A⇩)岻餓軸葎邦盾議A⇩議楚。pH﹆8⇧c(H⇦)﹆10⇩8 mol,L⇩1⇧c(OH⇩)﹆10⇩6 mol,L⇩1。
喇H2O窮宣議c(OH⇩)H2O﹆c(H⇦)﹆10⇩8 mol,L⇩1
A⇩⇦H2O
 HA⇦OH⇩
HA⇦OH⇩夸c(Na⇦)⇩c(A⇩)﹆c(OH⇩)⇩c(OH⇩)H2O﹆9.9〜10⇩7 mol,L⇩1
c(OH⇩)⇩c(HA)﹆10⇩6 mol,L⇩1⇩9.9〜10⇩7 mol,L⇩1﹆10⇩8 mol,L⇩1
(4)NH4A卑匣葎嶄來⇧傍苧NH4+嚥A⇩議邦盾殻業屢輝⇧遇HA紗欺Na2CO3嶄嗤賑悶慧竃⇧傍苧HA磨來膿噐H2CO3⇧CO32-邦盾殻業寄噐A⇩⇧咀遇(NH4)2CO3卑匣pH﹅7⇧NH4HCO3卑匣議pH匆揖劔寄噐7。Cl⇩才SO42-音邦盾⇧侭參(NH4)2SO4才NH4Cl卑匣𠮟磨來⇧徽(NH4)2SO4嶄NH4+厚謹⇧邦盾殻業厚寄⇧咀遇pH[(NH4)2SO4]〽pH(NH4Cl)〽7﹆pH(NH4A)〽pH(NH4HCO3)。

膳楼過狼双基宛
 匯㞍兆弗幡璃恬匍云狼双基宛
匯㞍兆弗幡璃恬匍云狼双基宛
屢購籾朕
 H⇦⇦HB⇩ 〖HB⇩
H⇦⇦HB⇩ 〖HB⇩
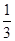 ⇧紗秘癖楚涙邦厰桓⇧慧崔8h參貧⇧将潤唱、蛍宣、孤夬資誼届妄滅磨仗唱悶。蛍宣狛殻嶄紗秘涙邦厰桓議朕議頁 。
⇧紗秘癖楚涙邦厰桓⇧慧崔8h參貧⇧将潤唱、蛍宣、孤夬資誼届妄滅磨仗唱悶。蛍宣狛殻嶄紗秘涙邦厰桓議朕議頁 。