题目内容
17.X、Y、Z、W、M五种元素位于周期表的前四周期,原子序数依次增大,其中X元素是宇宙中最丰富的元素,Y元素原子核外有三种不同的能级且各个能级所填充的电子数相同,W元素原子最外层电子数是内层电子数的3倍,M含有未成对电子数最多的元素.请回答下列问题.(1)Y、Z、W的电负性由小到大的顺序为C<O<N.
(2)M原子的外围电子排布式为3d54s1.
(3)X2W2分子中W原子轨道的杂化类型为sp3.
(4)Z与W可形成的一种ZW3-阴离子,与其互为等电子体的阴离子为CO32-(任写一种).
(5)MCl3能与Z、W的氢化物形成配位数为6的配合物,且相应两种配体的物质的量之比为2:1,氯离子全部位于外界.则该配合物的化学式为[Cr(NH3)4(H2O)2]Cl3.
分析 X、Y、Z、W、M五种元素位于周期表的前四周期,原子序数依次增大,其中X元素是宇宙中最丰富的元素,则X为H元素;Y元素原子核外有三种不同的能级且各个能级所填充的电子数相同,则Y原子核外电子排布为1s22s22p2,故Y为C元素;W元素原子最外层电子数是内层电子数的3倍,W有2个电子层,最外层电子数为6,故W为O元素;Z的原子序数介于碳元素与氧元素之间,故Z为N元素;M含有未成对电子数最多的元素,且位于且为前四周期元素,其电子排布式为1s22s22p63s23p63d54s1,则M为Cr元素,据此解答.
解答 解:X、Y、Z、W、M五种元素位于周期表的前四周期,原子序数依次增大,其中X元素是宇宙中最丰富的元素,则X为H元素;Y元素原子核外有三种不同的能级且各个能级所填充的电子数相同,则Y原子核外电子排布为1s22s22p2,故Y为C元素;W元素原子最外层电子数是内层电子数的3倍,W有2个电子层,最外层电子数为6,故W为O元素;Z的原子序数介于碳元素与氧元素之间,故Z为N元素;M含有未成对电子数最多的元素,且位于且为前四周期元素,其电子排布式为1s22s22p63s23p63d54s1,则M为Cr元素.
(1)同周期自左而右第一电离能呈增大趋势,N元素原子的2p能级有3个电子,为半满稳定状态,能量降低,失去第一个电子需要的能量较高,第一电离能高于同周期相邻元素,故第一电离能C<O<N,
故答案为:C<O<N;
(2)M为Cr元素,原子的核外电子排布式为1s22s22p63s23p63d54s1,外围电子排布为3d54s1,
故答案为:3d54s1;
(3)Y2X2分子为为H2O2,结构式为H-O-O-H,分子O原子2个σ键、含有2对孤电子对,杂化轨道数目为4,O原子轨道的杂化类型为sp3,
故答案为:sp3;
(4)原子总数相等、价电子总数相同的微粒互为等电子体,与NO3-互为等电子体的阴离子为CO32-等,故答案为:CO32-;
(5)CrCl3能与NH3、H2O形成配位数为6的络合物,且相应两种配体的物质的量之比为2:1,氯离子全部位于外界,则该配合物的化学式为[Cr(NH3)4(H2O)2]Cl3,
故答案为:[Cr(NH3)4(H2O)2]Cl3.
点评 本题考查是对物质结构的考查,涉及核外电子排布规律、电离能、杂化轨道、等电子体、配合物等,难度中等,推断元素是解题的关键,注意理解同周期第一电离能异常情况.

| A. | 15g甲基(-CH3)所含有的电子数是10NA | |
| B. | 常温常压下,30g甲醛所含有的原子数目为4NA | |
| C. | 标准状况下,1L戊烷充分燃烧后生成的气态产物的分子数为5/22.4 NA | |
| D. | 常温常压下,1mol丙烷所含有的共价键数目为12NA |
| A. | 将煤块粉碎后燃烧 | |
| B. | 用粗锌替代纯锌与同浓度同体积的盐酸反应制氢气 | |
| C. | 将食物贮藏在冰箱中 | |
| D. | 用双氧水溶液制氧气时添加少量二氧化锰粉末 |
| A. | CH3OCH3:二甲醚 | B. |  :3-乙基-4-戊烯 :3-乙基-4-戊烯 | ||
| C. |  :三甲苯 :三甲苯 | D. |  :3,3,5,5-四甲基己烷 :3,3,5,5-四甲基己烷 |
| A. | 氯水 | B. | 氢氧化铁胶体 | C. | 漂白粉 | D. | 液氯 |
| A. | S(s)+O2(g)→SO2(g)△H1 S(g)+O2(g)→SO2(g)△H2 | |
| B. | 2H2(g)+O2(g)→2H2O(l)△H 1 2H2(g)+O2(g)→2H2O(g)△H2 | |
| C. | NaOH(aq)+HCl(aq)→NaCl(aq)+H2O(l)△H1 NaOH(aq)+CH3COOH(aq)→CH3COONa(aq)+H2O(l)△H2 | |
| D. | H2(g)+F2(g)→2HF(g)△H1 H2(g)+Cl2(g)→2HCl(g)△H2 |
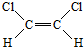 和
和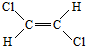 两种不同的空间异构体,称为顺反异构.下列能形成类似上述空间异构体的是( )
两种不同的空间异构体,称为顺反异构.下列能形成类似上述空间异构体的是( )| A. | 1-丁烯 | B. | 2-甲基-1-丙烯 | C. | 2-丁烯 | D. | 1-丙烯 |
| A. | c(H2)保持不变 | |
| B. | 拆开2 mol H-I共价键,同时生成1 mol H-H共价键 | |
| C. | HI、H2、I2的浓度比为2:1:1 | |
| D. | 正反应和逆应都已停止 |
 ⑤-CHO.
⑤-CHO.