题目内容
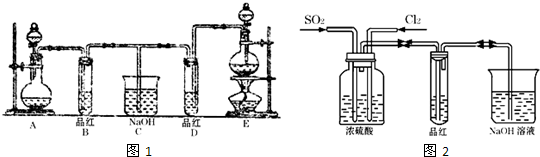
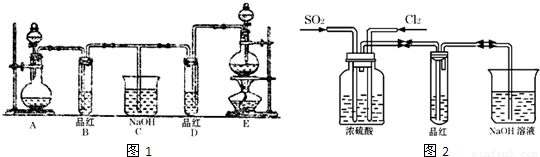
实验室用浓盐酸和MnO2是制取并探究Cl2化学性质,装置图下图:
(1)A是氯气发生装置,除了酒精的外还用到的玻璃仪器有
(2)从C装置出来的气体中含有CO2和HCl,写出C中反应的化学方程式
(3)同学们在实验中发现:若用稀盐酸代替浓盐酸与MnO2混合加热没有氯气生成.“影响氯气生成的原因是什么呢?”同学们作了如下探究:
①提出合理假设
假设1:Cl-的浓度对反应的影响;假设2:
②设计实验方案,进行实验.请在答题卡上写出实验步骤以及预期现象和结论.限选实验试剂:浓H2SO4、NaCl固体、MnO2固体、稀盐酸
| 实验序号 | 实验操作 | 预期现象和结论 |
| ① | ||
| ② |
分析:(1)根据制取氯气的反应条件及使用的试剂选择选择使用的玻璃仪器;
(2)根据反应物为氯气、水和C,生成物为二氧化碳和氯化氢写出反应的化学方程式;
(3)浓盐酸和稀盐酸的区别在于溶液中氢离子和氯离子浓度大小,可以分别设计实验方案证明是氯离子浓度影响反应还是氢离子浓度影响反应;证明氯离子对反应的影响,可以通过改变稀盐酸中氯离子浓度,观察是否产生黄绿色氯气;证明氢离子对反应的影响,可以改变稀盐酸中的氢离子浓度,观察是否产生黄绿色气体.
(2)根据反应物为氯气、水和C,生成物为二氧化碳和氯化氢写出反应的化学方程式;
(3)浓盐酸和稀盐酸的区别在于溶液中氢离子和氯离子浓度大小,可以分别设计实验方案证明是氯离子浓度影响反应还是氢离子浓度影响反应;证明氯离子对反应的影响,可以通过改变稀盐酸中氯离子浓度,观察是否产生黄绿色氯气;证明氢离子对反应的影响,可以改变稀盐酸中的氢离子浓度,观察是否产生黄绿色气体.
解答:解:(1)制取氯气的反应中,反应需要加热,用到酒精灯;反应物为浓盐酸和二氧化锰,浓盐酸盛放在分液漏斗中,二氧化锰盛放在圆底烧瓶中,还需要用到导管进行连接仪器,
故答案为:分液漏斗、圆底烧瓶、导管;
(2)C装置中的反应物为氯气、水和碳,生成物为氯化氢和二氧化碳,根据化学方程式书写原则写出化学方程式为:2Cl2+2H2O+C
4HCl+CO2↑,
故答案为:2Cl2+2H2O+C
4HCl+CO2↑;
(3)稀盐酸中含有的离子是氯离子和氢离子,故猜想2为H+的浓度对反应的影响,若证明氯离子的浓度对反应是否有影响,可增大氯离子的浓度,观察是否产生黄绿色气体,若证明氢离子浓度对反应是否有影响,可增大氢离子浓度,观察是否产生黄绿色气体氯气,因此实验方案如下:
①稀盐酸加入二氧化锰中,然后滴入氯化钠固体加热;若有黄绿色气体生成,则与氯离子浓度有关,若没有黄绿色气体生成,则与氯离子浓度无关;
②将将稀盐酸加入二氧化锰中,然后滴入浓硫酸,加热;若有黄绿色气体生成,则与氢离子浓度有关,若没有黄绿色气体生成,则与氢离子浓度无关;
故答案为:H+的浓度对反应的影响;
.
故答案为:分液漏斗、圆底烧瓶、导管;
(2)C装置中的反应物为氯气、水和碳,生成物为氯化氢和二氧化碳,根据化学方程式书写原则写出化学方程式为:2Cl2+2H2O+C
| ||
故答案为:2Cl2+2H2O+C
| ||
(3)稀盐酸中含有的离子是氯离子和氢离子,故猜想2为H+的浓度对反应的影响,若证明氯离子的浓度对反应是否有影响,可增大氯离子的浓度,观察是否产生黄绿色气体,若证明氢离子浓度对反应是否有影响,可增大氢离子浓度,观察是否产生黄绿色气体氯气,因此实验方案如下:
①稀盐酸加入二氧化锰中,然后滴入氯化钠固体加热;若有黄绿色气体生成,则与氯离子浓度有关,若没有黄绿色气体生成,则与氯离子浓度无关;
②将将稀盐酸加入二氧化锰中,然后滴入浓硫酸,加热;若有黄绿色气体生成,则与氢离子浓度有关,若没有黄绿色气体生成,则与氢离子浓度无关;
故答案为:H+的浓度对反应的影响;
| 将稀盐酸加入二氧化锰中,然后滴入氯化钠固体加热 | 若有黄绿色气体生成,则与氯离子浓度有关, 若没有黄绿色气体生成,则与氯离子浓度无关. | |
| 将稀盐酸加入二氧化锰中,然后滴入浓硫酸,加热 | 若有黄绿色气体生成,则与氢离子浓度有关, 若没有黄绿色气体生成,则与氢离子浓度无关. |
点评:本题考查了氯气的实验室制法及氯气的化学性质,题目难度较大,涉及了质量守恒定律及实验方案的设计,要求学生能够根据物质的不同点找出影响反应速率的因素,并且能够设计实验方案证明,本题旨在考查学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
回收的废旧锌锰于电池经过处理后得到锰粉(含MnO2、Mn(OH)2、Fe、氯化铵和黑炭等),由锰粉制取MnO2的步骤如图所示.
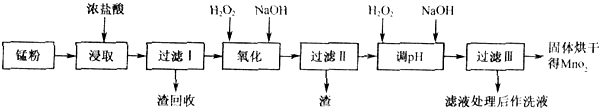
根据如图所示步骤并参考表格数据,回答下列问题.
生成氢氧化物沉淀的pH
(1)在加热条件下用浓盐酸浸取锰粉,所得溶液中含有Mn2+、Fe2+等.MnO2与浓盐酸反应的离子方程式为 .
(2)锰粉经浓盐酸浸取,过滤I除去不溶杂质后,向滤液中加入足量H2O2溶液,其作用是 .
(3)过滤Ⅰ所得滤液经氧化后,需加入NaOH溶液调节pH约为5.1,其目的是 .
(4)过滤Ⅱ所得滤液加入足量H2O2溶液并加入NaOH溶液调节pH约为9,使Mn2+氧化得到MnO2,反应的离子方程式为 .
(5)实验室进行过滤操作时.需要用到的玻璃仪器有 .

根据如图所示步骤并参考表格数据,回答下列问题.
生成氢氧化物沉淀的pH
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)2 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Mn(OH)2 | 8.3 | 9.8 |
(2)锰粉经浓盐酸浸取,过滤I除去不溶杂质后,向滤液中加入足量H2O2溶液,其作用是
(3)过滤Ⅰ所得滤液经氧化后,需加入NaOH溶液调节pH约为5.1,其目的是
(4)过滤Ⅱ所得滤液加入足量H2O2溶液并加入NaOH溶液调节pH约为9,使Mn2+氧化得到MnO2,反应的离子方程式为
(5)实验室进行过滤操作时.需要用到的玻璃仪器有
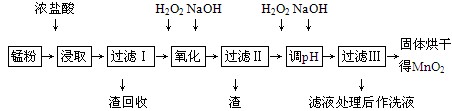
回收的废旧锌锰干电池经过处理后得到锰粉(含MnO2、Mn(OH)2、Fe、乙炔和黑炭等),由锰粉制取MnO2的步骤如下图所示。
生成氢氧化物沉淀的pH
|
物质 |
开始沉淀 |
沉淀完全 |
|
Fe(OH)3 |
2.7 |
3.7 |
|
Fe(OH)2 |
7.6 |
9.6 |
|
Mn(OH)2 |
8.3 |
9.8 |
根据上图所示步骤并参考表格数据,回答下列问题。
(1)在加热条件下用浓盐酸浸取锰粉,所得溶液中含有Mn2+、Fe2+等。MnO2与浓盐酸反应的离子方程式为___________________________________________
(2)锰粉经浓盐酸浸取,过滤Ⅰ除去不溶杂质后,向滤液中加入足量H2O2溶液,其作用是____________________________________________________________。
(3)过滤Ⅰ所得滤液经氧化后,需加入NaOH溶液调节pH约为5.1,其目的是___________________________________________________________。
(4)过滤Ⅱ所得滤液加入足量H2O2溶液并加入NaOH溶液调节pH约为9,使Mn2+氧化得到MnO2,反应的离子方程式为_____________________________________________。
(5)实验室进行过滤操作时,需要用到的玻璃仪器有________________________