题目内容
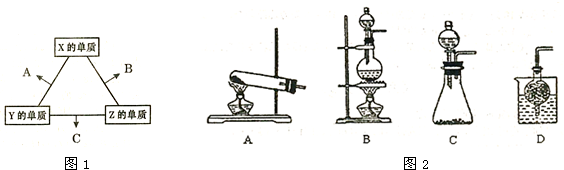
X、Y、Z三种短周期元素,它们之间的化合物有XY2、Z2Y、XY3、Z2Y2、Z2X等。已知Ym-与Zn+两种离子具有相同的电子层结构;Xm-比Ym-多一层电子。试完成:(1)X原子的原子结构示意图是_________________,它处于周期表中_________________周期_______________族。
(2)Z2Y2的电子式为_______________,Z2Y的电子式为_______________。
(3)XY3在标准状况下是针状晶体,它属于_______________晶体。又知XY3的水化物与Z2Y2反应可生成一种具有漂白作用的强氧化剂H2Y2,推测反应时的化学方程式为_____________
____________________________________________。
(4)Z2X属于晶体:Z2X的水溶液和XY3的水化物在溶液中反应的离子方程式是__________
____________________________________________。
(5)由X、Y、Z和氢四种元素所组成的两种化合物溶液,反应产生气体的离子方程式是
_____________________________________________。
解析:Xm-与Ym-带有相同电荷,可知X和Y位于同一主族,且能形成XY2和XY3型化合物。从Z2Y可知Y应显-2价。由此可推得X为S元素,Y为O元素。化学方程式为:NaHSO3+NaHSO4![]() Na2SO4+SO2↑+H2O。
Na2SO4+SO2↑+H2O。
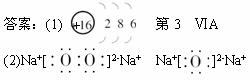
(3)分子 H2SO4+Na2O2![]() Na2SO4+H2O2
Na2SO4+H2O2
(4)离子 2H++S2-![]() H2S↑
H2S↑
(5)![]() +H+
+H+![]() SO2↑+H2O
SO2↑+H2O

练习册系列答案
相关题目