题目内容
常温下,用 0.1000 mol·L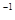 NaOH溶液滴定 20.00mL0.1000 mol·L
NaOH溶液滴定 20.00mL0.1000 mol·L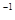
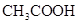 溶液所得滴定曲线如右图。下列说法正确的是
溶液所得滴定曲线如右图。下列说法正确的是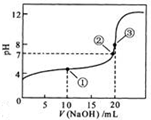
A.点①所示溶液中: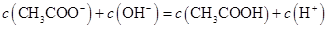 |
B.点②所示溶液中: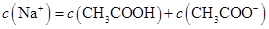 |
C.点③所示溶液中: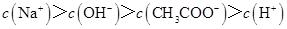 |
D.滴定过程中可能出现: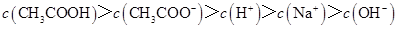 |
D
解析试题分析:A、点①所示溶液为醋酸和醋酸钠等浓度的混合液,将电荷守恒和物料守恒的式子相结合得c(CH3COO-)+2 c(OH-)= c(CH3COOH)+2 c(H+),错误;B、点②所示溶液呈中性,c(H+)=c(OH-),再根据电荷守恒得c(Na+)=c(CH3COO-),错误;C、点③所示溶液呈碱性,此时溶液为醋酸钠溶液,离子浓度的大小关系为c(Na+)> c(CH3COO-)> c(OH-)> c(H+),错误;D、在刚滴定时,加入氢氧化钠溶液很少,醋酸部分电离产生的氢离子与氢氧根离子结合成水可能会出现c(CH3COOH)> c(CH3COO-)> c(H+)> c(Na+)> c(OH-),正确,答案选D。
考点:考查酸碱混合液中离子浓度的大小比较及守恒规律的应用

在pH都等于9的NaOH和CH3COONa两种溶液中,设由水电离产生的OH-离子浓度分别为A mol·L-1与B mol·L-1,则A和B的关系为
| A.A>B | B.A=10-4B | C.B=10-4A | D.A=B |
下列各溶液中,微粒的物质的量浓度关系正确的是( )
| A.常温下,将pH=2的盐酸和pH=12的氨水等体积混合后:c(NH4+)>c(Cl-)> c(OH-)>c(H+) |
| B.0.1 mol·L-1 Na2CO3溶液:c(Na+)=2c(HCO3-)+2c(CO32¯)+2c(H2CO3) |
| C.0.1 mol·L-1 NH4Cl溶液:c(NH4+)=c( Cl-) |
| D.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液: c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
已知在25℃时,氯化银的Ksp=1.8×10-10,现将足量氯化银分别放入下列溶液中,相同温度下c(Ag+)最大的是
| A.100mL蒸馏水 | B.100mL 0.2mol·L-1 AgNO3 |
| C.100 mL 0.1mol·L-1AlCl3 | D.100mL 0.1 mol·L-1盐酸 |
pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值。如某溶液溶质的浓度为:1×10-3mol·L-1,则该溶液中溶质的pC=3。下列表达正确的是
| A.某温度下任何电解质的水溶液中,pC(H+) +pC(OH-)=14 |
| B.0.01mol/L的CaCl2溶液中逐渐滴加纯碱溶液,滴加过程中pC(Ca2+)逐渐减小 |
| C.用0.01mol/L的盐酸滴定某浓度的NaOH溶液,滴定过程中pC(H+)逐渐增大 |
| D.某温度下,AB难溶性离子化合物的Ksp=1.0×10-10, 其饱和溶液中pC(A+) +pC((B-)=10 |
已知CuSO4溶液分别与Na2CO3溶液、Na2S溶液的反应情况如下:
(1)CuSO4+Na2CO3:Cu2++CO32-+H2O=Cu(OH)2↓+CO2↑
(2)CuSO4+Na2S: Cu2++S2-=CuS↓
下列几种物质的溶解度大小的比较中,正确的是
| A.CuS<Cu(OH)2<CuCO3 | B.CuCO3<Cu(OH)2<CuS |
| C.CuS<CuCO3<Cu(OH)2 | D.Cu(OH)2<CuCO3<CuS |
25°C时,弱酸的电离平衡常数如下表:
| 弱酸 | CH3COOH | HCN | H2CO3 |
| Ka | 1.8×10-5 | 4.9×10-10 | K1:4.3×10-7 K2:5.6×10-11 |
下列有关说法正确的是( )
A.等物质的量浓度的各溶液的pH关系为:
pH(NaCN)>pH(Na2CO3)>pH(CH3COONa)
B.a mol·L-1HCN与b mol·L-1 NaOH溶液等体积混合后所得溶液中c(Na+)>c(CN-),则a一定小于b
C.往冰醋酸中逐滴加水,溶液导电能力增大
D.NaHCO3和Na2CO3的混合液中:c(Na+)+c(H+)=c(OH-)+c(HCO3—)+2c(CO32—)
室温下,在pH为5的NH4Cl溶液、pH为9的NaHCO3溶液和pH为5的盐酸中,水的电离度分别为:α1、α2、α3,它们之间的大小关系是 ( )
| A.α1<α2<α3 | B.α1=α2>α3 | C.α1>α2>α3 | D.无法判断 |