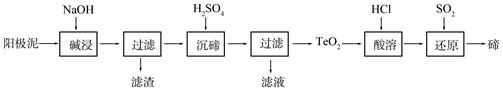
题目内容
(10分)有三份不同质量的铁粉样品①②③,甲、乙、丙三位同学各取一份样品分别与含有0.8molHNO3的稀硝酸反应,反应后硝酸和铁均无剩余,且硝酸的还原产物只有NO。据此回答下列问题:
(1)甲取样品①,反应后的溶液中铁只以Fe3+离子的形式存在,则样品①的质量为 g。
(2)乙取样品②,反应后的溶液中既含有Fe3+、又含有Fe2+离子,则样品②的质量(设为ag)范围是 。
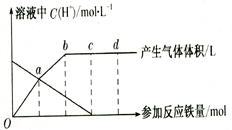
(3)丙取样品③,将其慢慢加入到稀硝酸中,并不断搅拌,反应过程中溶液里Fe3+、Fe2+、NO3—三种离子中的两种离子的物质的量的变化曲线如下图所示,则该曲线表示的是 物质的量变化的曲线,请你在此图中再画出另外种离子的物质的量的变化曲线。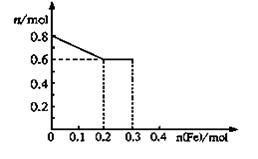
⑴11.2g ⑵11.2<a<16.8 ⑶NO3- 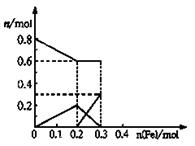
解析试题分析:⑴设Fe的物质的量是x,则生成硝酸铁也是x,所以被还原的硝酸是0.8mol-3x。根据电子的得失守恒可知,3x=3×(0.8mol-3x),解得x=0.2mol,所以铁的质量是0.2mol×56g/mol=11.2g。
⑵如果铁的氧化产物是亚铁离子,则生成硝酸亚铁是x,所以被还原的硝酸是0.8mol-2x。根据电子的得失守恒可知,2x=3×(0.8mol-2x),解得x=0.3mol,所以铁的质量是0.3mol×56g/mol=16.8g。因此如果是反应后的溶液中既含有Fe3+,又含有Fe2+,则样品②的质量是11.2<a<16.8。
⑶由于最初溶液中NO3-的物质的量就是0.8mol,所以曲线表示的是NO3-的物质的量变化的曲线;根据反应的方程式Fe+4HNO3=Fe(NO3)3+NO↑+2H2O、2Fe(NO3)3+Fe= 3Fe(NO3)2可知,铁离子的最大值是0.2mol。如果继续加入铁,则开始生成亚铁离子,亚铁离子的最大值是0.3mol;综上分析便可画出Fe3+、Fe2+离子的物质的量的变化曲线。
考点:考查铁与硝酸反应的化学计算。

固体NH5属于离子晶体。它与水反应的化学方程式为:NH5+H2O→NH3·H2O+H2↑,它也能跟乙醇发生类似的反应,并都产生氢气。下列有关NH5叙述正确的是
| A.与水反应时,水作氧化剂 | B.NH5中N元素的化合价为+5价 |
| C.1 mol NH5中含有5NA个N—H键 | D.与乙醇反应时,NH5被还原 |
已知Iˉ、Fe2+、SO2、Clˉ、H2O2均有还原性,它们在酸性溶液中还原性的强弱顺序为Clˉ< Fe2+< H2O2< Iˉ< SO2。则下列反应不能发生的是
| A.2Fe3++SO2+2H2O=2Fe2++SO42ˉ+4H+ |
| B.Cl2+SO2+2H2O=H2SO4+2HCl |
| C.H2O2+2H++ SO42ˉ=SO2↑+O2↑+2H2O |
| D.2I2+H2O2=2H2O+O2↑+4 Iˉ |

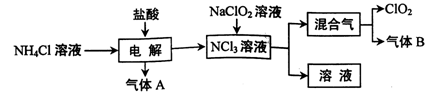
 (1)焙烧的过程中采用的是“逆流焙烧”的措施,则该措施的优点是:①_______________
(1)焙烧的过程中采用的是“逆流焙烧”的措施,则该措施的优点是:①_______________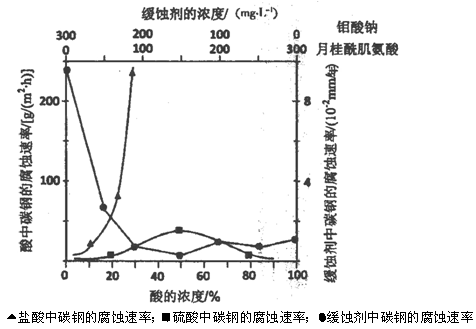
 Lix(MoS2)n。则电池放电时的正极反应式是:___________________________________。
Lix(MoS2)n。则电池放电时的正极反应式是:___________________________________。