题目内容
下列说法正确的是
| A.2.24 L CO2中共有的原子数为0.3×6.02×1023 |
B.1.8 g N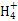 共有的质子数为6.02×1023 共有的质子数为6.02×1023 |
| C.1 mol重水分子所含中子数为10×6.02×1023 |
| D.7.8 g Na2O2中含有的阴离子数为0.2×6.02×1023 |
C
标准状况下,2.24 L CO2中含有的原子数为0.3×6.02×1023,A错误;1个N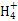 含有11个质子,1.8 g N
含有11个质子,1.8 g N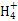 含有的质子数为1.1×6.02×1023,B错误;1个重水分子含有10个中子,1 mol重水分子所含中子数为10×6.02×1023,C正确;Na2O2中阴离子为
含有的质子数为1.1×6.02×1023,B错误;1个重水分子含有10个中子,1 mol重水分子所含中子数为10×6.02×1023,C正确;Na2O2中阴离子为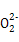 ,7.8 g Na2O2含有的阴离子数为0.1×6.02×1023,D错误。
,7.8 g Na2O2含有的阴离子数为0.1×6.02×1023,D错误。
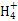 含有11个质子,1.8 g N
含有11个质子,1.8 g N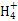 含有的质子数为1.1×6.02×1023,B错误;1个重水分子含有10个中子,1 mol重水分子所含中子数为10×6.02×1023,C正确;Na2O2中阴离子为
含有的质子数为1.1×6.02×1023,B错误;1个重水分子含有10个中子,1 mol重水分子所含中子数为10×6.02×1023,C正确;Na2O2中阴离子为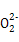 ,7.8 g Na2O2含有的阴离子数为0.1×6.02×1023,D错误。
,7.8 g Na2O2含有的阴离子数为0.1×6.02×1023,D错误。
练习册系列答案
相关题目
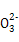 )="1" mol/L,则c(Na+)="2" mol/L
)="1" mol/L,则c(Na+)="2" mol/L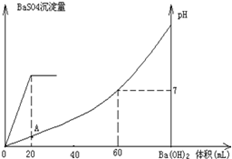
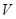 [Ba(OH)2(aq)]=10mL时,发生反应的离子方程式为:Ba2++SO
[Ba(OH)2(aq)]=10mL时,发生反应的离子方程式为:Ba2++SO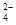 ═BaSO4↓
═BaSO4↓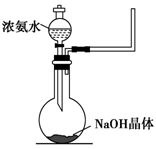
 NH4++OH-,NaOH晶体使该可逆反应的平衡向左移动
NH4++OH-,NaOH晶体使该可逆反应的平衡向左移动