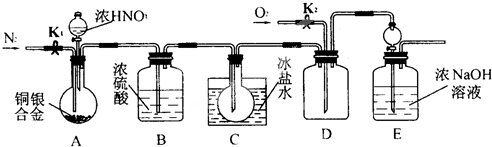
题目内容
13.A、B、C、D、E是五种中学常见的单质,已知A、B、C、D在常温下均为气态,其中D能分别跟A、B、C在一定条件下两两化合,生成化合物X、Y、Z;A与B、C均不能直接化合,有关的转化关系如下图所示(反应条件均已略去)回答下列问题:(1)Z分子的空间构型为三角锥形
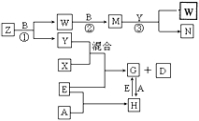 (2)反应③中被氧化的物质与被还原的物质的物质的量之比为2:1
(2)反应③中被氧化的物质与被还原的物质的物质的量之比为2:1(3)Z和W在催化剂作用下,反应生成C和Y,这是一个很有实际意义的反应,可以消除W对环境的污染,该反应的方程式为4NH3+6NO$\frac{\underline{催化剂}}{△}$5N2+6H2O.
(4)将过量的E加到N的稀溶液中,若过程中转化的电子数目为3.02×1023个,则参加反应的E的物质的量为0.25mol.
(5)将Z和N反应后的产物溶于水中,则溶液的pH值(填“<”或“>”)<7,其原因是(用离子方程式表示)NH4++H2O═NH3•H2O.
分析 A、B、C、D在常温下是气体单质,常见的气体单质只有H2、N2、O2、F2、Cl2 五种,其中D能分别跟A、B、C在一定条件下两两化合,可推出D为H2,那么对应的氢化物可为NH3、H2O、HF(或者HCl).由Y+X+E→G+H2,可知E为金属,又因为G?H,所以E为变价金属Fe,那么Y+X应为常见的盐酸,那么A为Cl2,X为HCl,C为N2,Z为NH3,B为O 2,Y为H2O,由转化关系可知W为NO,M为NO2,N为HNO3,G为FeCl2,H为FeCl3,结合对应物质的性质以及题目要求解答该题.
解答 解:A、B、C、D在常温下是气体单质,常见的气体单质只有H2、N2、O2、F2、Cl2 五种,其中D能分别跟A、B、C在一定条件下两两化合,可推出D为H2,那么对应的氢化物可为NH3、H2O、HF(或者HCl).由Y+X+E→G+H2,可知E为金属,又因为G?H,所以E为变价金属Fe,那么Y+X应为常见的盐酸,那么A为Cl2,X为HCl,C为N2,Z为NH3,B为O 2,Y为H2O,由转化关系可知W为NO,M为NO2,N为HNO3,G为FeCl2,H为FeCl3,
(1)Z为NH3,为三角锥形分子,故答案为:三角锥形;
(2)反应③为NO2+H2O=2HNO3+NO,由化合价变化可知被氧化的物质与被还原物质的物质的量之比为2:1,故答案为:2:1;
(3)Z为NH3,W为NO,在催化剂作用下,反应生成氮气和水,方程式为4NH3+6NO$\frac{\underline{催化剂}}{△}$5N2+6H2O,故答案为:4NH3+6NO$\frac{\underline{催化剂}}{△}$5N2+6H2O;
(4)过量的Fe和HNO3 反应生成Fe2+,若过程中转化的电子数目为3.02×1023个,则转移0.5mol电子,参加反应的Fe为0.25 mol,
故答案为:0.25;
(5)Z与N反应后的产物为NH4NO3,为强酸弱碱盐,水解呈酸性,pH<7,离子方程式为NH4++H2O═NH3•H2O,故答案为:<;NH4++H2O═NH3•H2O.
点评 本题考查无机物的推断,明确框图中物质的转化及物质的性质是解答本题的关键,转化图中G与H的转化是推断的突破口,然后利用化学用语、氧化还原反应、盐类水解等知识即可解答.

| A. | 无水硫酸铜、蔗糖 | B. | 硅胶、硫酸亚铁 | C. | 食盐、硫酸亚铁 | D. | 生石灰、食盐 |
| A. | 氢氧化铁胶体滴加盐酸 | B. | 四羟基合铝酸钠溶液中加盐酸 | ||
| C. | 氯化铝溶液中滴加氢氧化钠溶液 | D. | 氯化铝溶液中滴加氨水 |
| A. | $\frac{a}{b}$=$\frac{1}{4}$ | B. | $\frac{a}{b}$=$\frac{3}{8}$ | C. | $\frac{1}{4}$≤$\frac{a}{b}$≤$\frac{3}{8}$ | D. | $\frac{a}{b}$的值无法确定 |
| A. | a=b=c | B. | c>a>b | C. | b>a>c | D. | a>c>b |

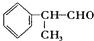
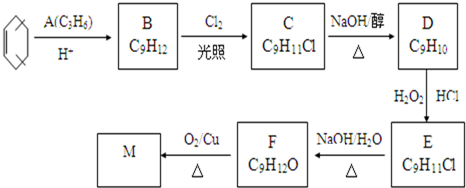
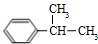 ;
;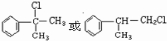 ;
;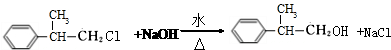 .
.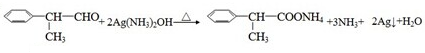 .
. .
.