题目内容
某学习小组为了探究 BrO3-+5Br-+6H+=3Br2 +3H2O 反应速率(v)与反应物浓度的关系,在20℃进行实验,所得的数据如下表:zxxk
 实验编号 实验编号相关数据 | ① | ② | ③ | ④ | ⑤ |
| c(H+)/ mol · L-1 | 0.008 | 0.008 | 0.004 | 0.008 | 0.004 |
| c(BrO3-)/ mol· L-1 | 0.001 | 0.001 | 0.001 | 0.002 | 0.002 |
| c(Br-)/ mol· L-1 | 0.10 | 0.20 | 0.20 | 0.10 | 0.40 |
| v / mol· L-1· s-1 | 2.4×10-8 | 4.8×10-8 | 1.2×10-8 | 4.8×10-8 | v1 |
下列结论不正确的是
A.若温度升高到40℃,则反应速率增大
B.实验②、④,探究的是c(BrO3-)对反应速率的影响
C.若该反应速率方程为v ="k" ca(BrO3-)cb(Br-)cc(H+)(k为常数),则c =2
D.实验⑤中,v1 =4.8×10-8 mol· L-1· s-1
B
解析试题分析:A、温度升高,反应速率增大,正确;B、实验②、④,Br?、BrO3?浓度不同,无法探究c(BrO3-)对反应速率的影响,错误;C、实验②H+浓度为③的2倍,其他条件都相同,速率②是③的4倍,所以c=2,正确;D、实验②Br?是实验①的2倍,速率也是2倍,可得a=1,实验⑤H+是④的1/2,Br?⑤是④的4倍,则速率④=⑤,正确。
考点:本题考查化学速率的计算、条件对速率的影响。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
在密闭容器中进行如下反应:X2(g)+Y2(g) 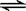 2Z(g)这是可逆反应,已知X2,Y2,Z的起始浓度分别为0.1摩尔/升,0.3摩尔/升,0.2摩尔/升,在一定条件下当反应达到平衡时,各物质浓度有可能是
2Z(g)这是可逆反应,已知X2,Y2,Z的起始浓度分别为0.1摩尔/升,0.3摩尔/升,0.2摩尔/升,在一定条件下当反应达到平衡时,各物质浓度有可能是
| A.Z为0.3摩尔/升 | B.Y2为0.4摩尔/升 |
| C.X2为0.2mol/L | D.Z为0.4摩尔/升 |
图中表示外界条件(T、p)的变化对下列反应的影响:L(s)+G(g) 2R(g)△H>0,y 轴表示的是
2R(g)△H>0,y 轴表示的是
| A.平衡时,混合气中R的百分含量 | B.G的转化率 |
| C.平衡时,混合气中G的百分含量 | D.L的转化率 |
汽车尾气中的有毒气体NO和CO,在一定条件下可发生反应生成N2和CO2。下列关于此反应的说法中,正确的是( )
| A.减小压强能增大反应速率 |
| B.增大压强能减小反应速率 |
| C.使用适当的催化剂能增大反应速率 |
| D.升高温度对反应速率无影响 |
PCl3和PCl5都是重要的化工原料。将PCl3(g)和Cl2(g)充入体积不变的2 L密闭容器中,在一定条件下发生下述反应,10 min时达到平衡:PCl3(g) + Cl2(g) PCl5(g)有关数据如下,下列判断不正确的是
PCl5(g)有关数据如下,下列判断不正确的是
| | PCl3(g) | Cl2(g) | PCl5(g) |
| 初始浓度(mol/L) | 2.0 | 1.0 | 0 |
| 平衡浓度(mol/L) | c1 | c2 | 0.4 |
A.10 min内,v(Cl2) =" 0.04" mol/(L·min)
B.当容器中Cl2为1.2 mol时,反应达到平衡
C.若升高温度(T1<T2)时,该反应平衡常数减小,则平衡时PCl3的
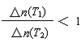
D.平衡后移走2.0 mol PCl3和1.0 molCl2,在相同条件下再达平衡时,c(PCl5)<0.2 mol/L
一定温度下,在一容积不变的密闭容器中发生的可逆反应2X(g)  Y(g)+Z(s),以下能说明反应达到平衡标志的是( )
Y(g)+Z(s),以下能说明反应达到平衡标志的是( )
| A.混合气体的压强不再变化 |
| B.X、Y、Z的物质的量之比为2:1:1 |
| C.单位时间内生成lmolY的同时分解2mol X |
| D.X的分解速率与Y的消耗速率相等 |
下列反应达到平衡后,升高温度可以使混合气体平均相对分子质量增大的是( )
A.H2(g)+I2(g)  2HI(g) ΔH<0 2HI(g) ΔH<0 |
B.4NH3(g)+5O2(g) 4NO(g)+6H2O(g) ΔH<0 4NO(g)+6H2O(g) ΔH<0 |
C.N2(g)+3H2(g)  2NH3(g)ΔH<0 2NH3(g)ΔH<0 |
D.2SO3(g) 2SO2(g)+O2(g) ΔH>0 2SO2(g)+O2(g) ΔH>0 |
 2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下表和下图表示:
2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下表和下图表示:

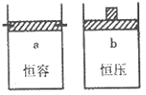
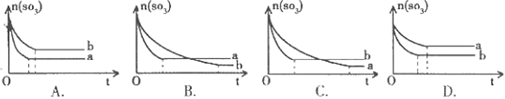
 2SO2(g)+O2(g),两容器中三氧化硫物质的量随时间(t)变化的示意图为
2SO2(g)+O2(g),两容器中三氧化硫物质的量随时间(t)变化的示意图为