题目内容
向200mL 6mol?L-1盐酸中加入一定量的纯净CaCO3,产生气体的体积随时间的变化曲线如图所示(气体体积均在标准 状况下测定).
请回答下列问题: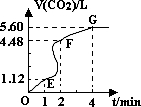
(1)设OE段的反应速率为υ1,EF段的反应速率为υ2,FG段的反应速率为υ3,则υ1、υ2、υ3从大到小的顺序为
(2)为了减缓上述反应的速率,欲向该溶液中加入下列物质,你认为可行的是
A、蒸馏水 B、氯化钾固体 C、氯化钠溶液 D、浓盐酸
(3)加入CaCO3的质量为
(4)若反应过程中溶液体积的变化忽略不计,则EF段用盐酸表示的化学反应速率υ(HCl)=
请回答下列问题:

(1)设OE段的反应速率为υ1,EF段的反应速率为υ2,FG段的反应速率为υ3,则υ1、υ2、υ3从大到小的顺序为
v2>v1>v3
v2>v1>v3
.(2)为了减缓上述反应的速率,欲向该溶液中加入下列物质,你认为可行的是
AC
AC
(填字母).A、蒸馏水 B、氯化钾固体 C、氯化钠溶液 D、浓盐酸
(3)加入CaCO3的质量为
25g
25g
.(4)若反应过程中溶液体积的变化忽略不计,则EF段用盐酸表示的化学反应速率υ(HCl)=
1.5mol?L-1?min-1
1.5mol?L-1?min-1
.分析:(1)单位时间内生成气体的体积越大,反应速率越大;
(2)减缓反应速率,应减小溶液的浓度;
(3)根据生成二氧化碳的体积计算二氧化碳的物质的量,根据反应方程式计算碳酸钙的物质的量,进而计算质量.
(4)根据v=
计算反应速率.
(2)减缓反应速率,应减小溶液的浓度;
(3)根据生成二氧化碳的体积计算二氧化碳的物质的量,根据反应方程式计算碳酸钙的物质的量,进而计算质量.
(4)根据v=
| c |
| t |
解答:解:(1)从图象可知,单位时间内生成的气体EF段>OE段>FG段,单位时间内生成气体的体积越大,反应速率越大,则
v2>v1>v3,故答案为:v2>v1>v3;
(2)A、加入蒸馏水,溶液的浓度减小,反应速率减小,故A正确;
B、氯化钾固体对溶液的浓度无影响,且KCl不参加反应,所以速率不变,故B错误;
C、加入氯化钠溶液,减小盐酸的浓度,反应速率减小,故C正确;
D、加入浓盐酸,盐酸的浓度增大,反应速率增大,故D错误,
故答案为:AC.
(3)当反应进行到4min时,生成气体的体积不变,说明碳酸钙完全反应,
则有:CaCO3+2HCl═CaCl2+CO2↑+H2O,
100g 22.4L
x 5.60L
则有:x=
=25g,
故答案为:25g.
(4)EF段生成二氧化碳的体积为4.48L-1.12L=3.36L,
CaCO3+2HCl═CaCl2+CO2↑+H2O
2mol 22.4L
n 3.36L
则:n=
=0.3mol,
消耗盐酸的浓度为c(HCl)=
=1.5mol/L,
所以EF段用盐酸表示的化学反应速率v(HCl)=
=1.5mol?L-1?min-1,
故答案为:1.5mol?L-1?min-1.
v2>v1>v3,故答案为:v2>v1>v3;
(2)A、加入蒸馏水,溶液的浓度减小,反应速率减小,故A正确;
B、氯化钾固体对溶液的浓度无影响,且KCl不参加反应,所以速率不变,故B错误;
C、加入氯化钠溶液,减小盐酸的浓度,反应速率减小,故C正确;
D、加入浓盐酸,盐酸的浓度增大,反应速率增大,故D错误,
故答案为:AC.
(3)当反应进行到4min时,生成气体的体积不变,说明碳酸钙完全反应,
则有:CaCO3+2HCl═CaCl2+CO2↑+H2O,
100g 22.4L
x 5.60L
则有:x=
| 100g×5.60L |
| 22.4L |
故答案为:25g.
(4)EF段生成二氧化碳的体积为4.48L-1.12L=3.36L,
CaCO3+2HCl═CaCl2+CO2↑+H2O
2mol 22.4L
n 3.36L
则:n=
| 2mol×3.36L |
| 22.4L |
消耗盐酸的浓度为c(HCl)=
| 0.3mol |
| 0.2L |
所以EF段用盐酸表示的化学反应速率v(HCl)=
| 1.5mol/L |
| 1min |
故答案为:1.5mol?L-1?min-1.
点评:本题考查化学反应速率计算、比较以及影响因素的判断,题目难度不大,注意计算的方法和影响因素有哪些.

练习册系列答案
相关题目
(5分)向200mL 6mol·L-1盐酸中加入一定量的纯净CaCO3,产生气体的体积随时间的变化曲线如图所示(气体体积均在标准状况下测定)。
请回答下列问题:
(1)设OE段的反应速率为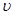 1,EF段的反应速率为
1,EF段的反应速率为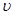 2,FG段的反应速率为
2,FG段的反应速率为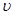 3,则
3,则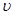 1、
1、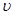 2、
2、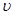 3从大到小的顺序为 。
3从大到小的顺序为 。
(2)为了减缓上述反应的速率,欲向该溶液中加入下列物质,你认为可行的是 (填字母)。
| A.蒸馏水 | B.氯化钾固体 |
| C.氯化钠溶液 | D.浓盐酸 |
(4)若反应过程中溶液体积的变化忽略不计,则EF段用盐酸表示的化学反应速率
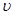 (HCl)= 。
(HCl)= 。 ( 8分 )向200mL 6mol·L-1盐酸中加入一定量的纯净CaCO3,产生气体的体积随时间的变化曲线如图所示(气体体积均在标准状况下测定)。请回答下列问题: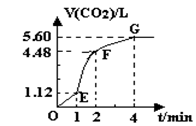
(1)设OE段的反应速率为v1,EF段的反应速率为v2,FG段的反应速率为v3,则v1、v2、v3从大到小的顺序为
(2)为了减缓上述反应的速率,欲向该溶液中加入下列物质,你认为可行的是 (填字母)。
| A.蒸馏水 | B.氯化钾固体 | C.氯化钠溶液 | D.浓盐酸 |
(4)若反应过程中溶液体积的变化忽略不计,则EF段用盐酸表示的化学反应速率V(HCl)== 。
 A、蒸馏水 B、氯化钾固体 C、氯化钠溶液 D、浓盐酸
A、蒸馏水 B、氯化钾固体 C、氯化钠溶液 D、浓盐酸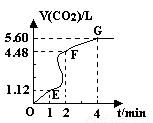 A、蒸馏水 B、氯化钾固体 C、氯化钠溶液 D、浓盐酸
A、蒸馏水 B、氯化钾固体 C、氯化钠溶液 D、浓盐酸