题目内容
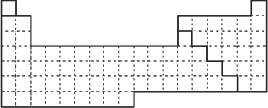
下图是元素周期表的框架
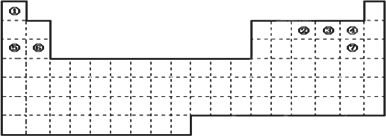
(1)请在上面元素周期表中画出金属元素与非金属元素的分界线.
(2)依据元素周期表回答下列问题:
A.周期表中的元素⑤和元素⑥的最高价氧化物的水化物碱性强弱顺序是________(用化学式表示).
B.周期表中的元素④和元素⑦的氢化物的熔、沸点高低顺序是________(用化学式表示).
C.①~⑦元素的单质,在常温下化学性质稳定,通常可用作保护气的是________(填写结构式).
D.在上面元素周期表中全部是金属元素的主族是________;全部是非金属元素的主族是________(填写字母a、b、c、d).
a.ⅠA族
b.ⅡA族
c.ⅥA族
d.ⅦA族
(3)已知甲元素位于第三周期,且其原子半径为同周期金属元素中原子半径最小的,请写出甲的氧化物与NaOH溶液反应的离子方程式________;
(4)请写出仅用①②④三种元素形成离子化合物的电子式________.若用球棍模型表示①和③形成的化合物的分子结构,应该是________.

(5)在120℃下1 g①的单质在足量③的单质中完全燃烧,放出的热量为a kJ;请写出此条件下①的单质燃烧的热化学方程式________;
①、③两种元素的单质已被应用于字宙飞船的燃料电池中,如图所示,两个电极均由多孔性碳构成,通入的两种单质由孔隙逸出并在电极表面放电.
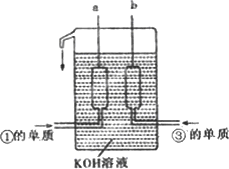
请回答:b是电池的________极;a电极上的电极反应式是________.
解析:
|
(1)如图.
图(2分) (2)A.NaOH>Mg(OH)2(2分) B.HF>HCl(2分) C. D.b;(1分) d(1分) (3)Al2O3+2OH-=2AlO2-+H2O(2分) (4) (5)H2(g)+1/2O2(g)=H2O(l) △H=-2a kJ/mol(2分) 正极(1分) H2-2e-+2OH-=2H2O(2分) |

 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案