题目内容
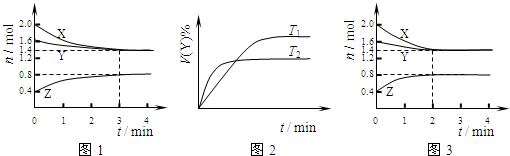
T℃时在2L容积不变的密闭容器中使X(g)与Y(g)发生反应生成Z(g).反应过程中X、Y、Z的物质的量变化如图1所示;若保持其他条件不变,温度分别为T1和T2时,Y的体积百分含量与时间的关系如图2所示.则下列结论错误的是( )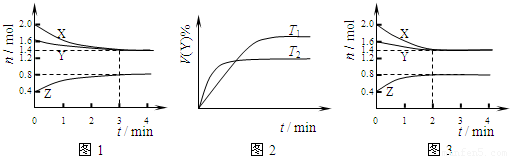
A.容器中发生的反应可表示为:3X(g)+Y(g)?2Z(g)
B.保持其他条件不变,升高温度,化学平衡向逆反应方向移动
C.反应进行前4 min内,用X表示的反应速率 v(X)=0.075mol?-1
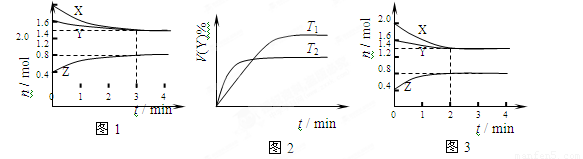
D.若改变反应条件,使反应进程如图3所示,则改变的条件是使用催化剂
【答案】分析:A、由图1可知,X、Y的物质的量减小,为反应物,Z的物质的量增大,为生成物,根据物质的量变化量之比等于化学计量数之比,确定化学计量数,反应最后各物质的物质的量不变,为可逆反应,据此书写.
B、由图2可知,温度T2到达平衡需要的时间较短,故T2>T1,温度越高Y的含量降低,升高温度平衡向正反应方向移动;
C、由图1可知,3min是反应达平衡,X的物质的量变化量为2.0mol-1.4mol=0.6mol,根据v= 计算v(X);
计算v(X);
D、图3与图1相比,平衡时各组分的物质的量不变,到达平衡时间缩短,说明改变条件,增大反应速率,平衡不移动,使用催化剂满足,结合反应方程式判断改变压强是否满足.
解答:解:A、由图1可知,X、Y的物质的量减小,为反应物,△n(X)=2.0mol-1.4mol=0.6mol,△n(Y)=1.6mol-1.4mol=0.2mol,Z的物质的量增大,为生成物,△n(Z)=0.8mol-0.4mol=0.4mol,故X、Y、Z的化学计量数之比为0.6mol:0.2mol:0.4mol=3:1:2,反应最后各物质的物质的量不变,为可逆反应,故该反应为3X(g)+Y(g)?2Z(g),故A正确;
B、由图2可知,温度T2到达平衡需要的时间较短,故T2>T1,温度越高Y的含量降低,升高温度平衡向正反应方向移动,说明正反应是吸热反应,故B错误;
C、由图1可知,3min是反应达平衡,X的物质的量变化量为2.0mol-1.4mol=0.6mol,故v(X)= =0.075mol?(L?min)-1,故C正确;
=0.075mol?(L?min)-1,故C正确;
D、图3与图1相比,平衡时各组分的物质的量不变,到达平衡时间缩短,说明改变条件,增大反应速率,平衡不移动,该反应正反应是气体体积减小的反应,增大压强平衡向正反应移动,不可能是增大压强,故改变条件是使用催化剂,故D正确;
故选B.
点评:考查化学平衡的图象及有关计算、平衡移动、化学反应速率有关计算等,难度中等,根据图象分析曲线变化特点,结合平衡移动解答.
B、由图2可知,温度T2到达平衡需要的时间较短,故T2>T1,温度越高Y的含量降低,升高温度平衡向正反应方向移动;
C、由图1可知,3min是反应达平衡,X的物质的量变化量为2.0mol-1.4mol=0.6mol,根据v=
 计算v(X);
计算v(X);D、图3与图1相比,平衡时各组分的物质的量不变,到达平衡时间缩短,说明改变条件,增大反应速率,平衡不移动,使用催化剂满足,结合反应方程式判断改变压强是否满足.
解答:解:A、由图1可知,X、Y的物质的量减小,为反应物,△n(X)=2.0mol-1.4mol=0.6mol,△n(Y)=1.6mol-1.4mol=0.2mol,Z的物质的量增大,为生成物,△n(Z)=0.8mol-0.4mol=0.4mol,故X、Y、Z的化学计量数之比为0.6mol:0.2mol:0.4mol=3:1:2,反应最后各物质的物质的量不变,为可逆反应,故该反应为3X(g)+Y(g)?2Z(g),故A正确;
B、由图2可知,温度T2到达平衡需要的时间较短,故T2>T1,温度越高Y的含量降低,升高温度平衡向正反应方向移动,说明正反应是吸热反应,故B错误;
C、由图1可知,3min是反应达平衡,X的物质的量变化量为2.0mol-1.4mol=0.6mol,故v(X)=
 =0.075mol?(L?min)-1,故C正确;
=0.075mol?(L?min)-1,故C正确;D、图3与图1相比,平衡时各组分的物质的量不变,到达平衡时间缩短,说明改变条件,增大反应速率,平衡不移动,该反应正反应是气体体积减小的反应,增大压强平衡向正反应移动,不可能是增大压强,故改变条件是使用催化剂,故D正确;
故选B.
点评:考查化学平衡的图象及有关计算、平衡移动、化学反应速率有关计算等,难度中等,根据图象分析曲线变化特点,结合平衡移动解答.

练习册系列答案
相关题目
 2Z(g)
2Z(g) 

 2Z(g)
2Z(g)