题目内容
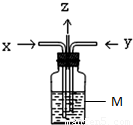
 如图,木炭与浓硫酸共热产生的气体X和铜跟浓稍酸反应产生的气体Y同时通入盛有足量BaCl2溶液的洗气瓶中.下列说法正确的是( )
如图,木炭与浓硫酸共热产生的气体X和铜跟浓稍酸反应产生的气体Y同时通入盛有足量BaCl2溶液的洗气瓶中.下列说法正确的是( )| A、洗气瓶中会产生BaCO3沉淀 | B、从导管Z中出来的气体中无CO2 | C、在Z导管口无红棕色气体出现 | D、洗气瓶中会产生BaSO4沉淀 |
分析:木炭与浓硫酸共热产生的X气体为CO2和SO2的混合气体,铜与浓硝酸反应产生的Y气体是NO2,同时通入时因NO2与水和SO2共同作用要产生SO42-和NO,NO在空气中又会生成红棕色的NO2,硫酸根离子与钡离子反应生成硫酸钡沉淀,以此解答该题.
解答:解:碳与浓硫酸共热产生的X气体为CO2和SO2的混合气体,铜与浓硝酸反应产生的Y气体是NO2,SO2+H2O+NO2=H2SO4+NO,故洗气瓶中产生的是硫酸钡沉淀,Z处逸出的气体有CO2和NO,NO遇到空气中的氧气生成了红棕色的NO2,
A.根据分析可知,洗气瓶中会产生硫酸钡沉淀,不是碳酸钡,故A错误;
B.从导管z出来的气体中为一氧化氮和二氧化碳,故B错误;
C.在z导管口一氧化氮与空气中的氧气反应生成红棕色的二氧化氮,有红棕色气体生成,故C错误;
D.洗气瓶中生成的硫酸根离子与钡离子反应生成沉淀硫酸钡,故正确;
故选D.
A.根据分析可知,洗气瓶中会产生硫酸钡沉淀,不是碳酸钡,故A错误;
B.从导管z出来的气体中为一氧化氮和二氧化碳,故B错误;
C.在z导管口一氧化氮与空气中的氧气反应生成红棕色的二氧化氮,有红棕色气体生成,故C错误;
D.洗气瓶中生成的硫酸根离子与钡离子反应生成沉淀硫酸钡,故正确;
故选D.
点评:本题考查了硝酸、浓硫酸的性质及二氧化硫、二氧化氮等物质的性质,题目难度不大,注意掌握浓硝酸、浓硫酸的化学性质,明确相关元素化合物具有的性质及反应现象.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 (2011?湖北模拟)如图,木炭与浓硫酸共热产生的气体x和铜跟浓硝酸反应产生的气体y同时通入盛有过量M的洗气瓶中,下列说法正确的是( )
(2011?湖北模拟)如图,木炭与浓硫酸共热产生的气体x和铜跟浓硝酸反应产生的气体y同时通入盛有过量M的洗气瓶中,下列说法正确的是( )
 (
(