��Ŀ����
��3.0mol M��2.5mol N�����2.0L�ĺ����ܱ������У�������Ӧ
3M (g) + N (g) xP (g) +2Q (g)��5min��Ӧ�ﵽƽ�⣬��֪M��ת����Ϊ50%��P�ķ�Ӧ����Ϊ0.15mol��L��1��min��1��������˵����ȷ���ǣ���
xP (g) +2Q (g)��5min��Ӧ�ﵽƽ�⣬��֪M��ת����Ϊ50%��P�ķ�Ӧ����Ϊ0.15mol��L��1��min��1��������˵����ȷ���ǣ���
3M (g) + N (g)
 xP (g) +2Q (g)��5min��Ӧ�ﵽƽ�⣬��֪M��ת����Ϊ50%��P�ķ�Ӧ����Ϊ0.15mol��L��1��min��1��������˵����ȷ���ǣ���
xP (g) +2Q (g)��5min��Ӧ�ﵽƽ�⣬��֪M��ת����Ϊ50%��P�ķ�Ӧ����Ϊ0.15mol��L��1��min��1��������˵����ȷ���ǣ���| A������ʽ��x=2 |
| B����ƽ���������ѹǿ�Ƿ�Ӧ��ʼʱ��2�� |
| C�����������ٳ���3.0molM��2.5molN������ƽ��ʱQ �����������С |
| D�������ڻ��������ܶȲ��ٱ仯��ƽ����Է����������ٱ仯������Ϊ�ﵽƽ��״̬�ı�־ |
C
P�ķ�Ӧ����Ϊ0.15mol��L��1��min��1��������P��0.15mol��L��1��min��1��2L��5min��1.5mol��M��ת����Ϊ50%��������M��1.5mol������x��3��A����ȷ��ƽ��ʱMNPQ�����ʵ����ֱ���1.5mol��2.0mol��1.5mol��1.0mol�����Դ�ƽ���������ѹǿ�Ƿ�Ӧ��ʼʱ��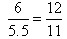 ��B����ȷ�����������ٳ���3.0molM��2.5molN���൱������ѹǿ���ƻ����淴Ӧ�����ƶ�������Q �����������С��C��ȷ���ܶ��ǻ�����������������ݻ��ı�ֵ���ڷ�Ӧ�������������ݻ�ʼ���Dz���ģ�����ѡ��D����ȷ����ѡC��
��B����ȷ�����������ٳ���3.0molM��2.5molN���൱������ѹǿ���ƻ����淴Ӧ�����ƶ�������Q �����������С��C��ȷ���ܶ��ǻ�����������������ݻ��ı�ֵ���ڷ�Ӧ�������������ݻ�ʼ���Dz���ģ�����ѡ��D����ȷ����ѡC��
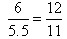 ��B����ȷ�����������ٳ���3.0molM��2.5molN���൱������ѹǿ���ƻ����淴Ӧ�����ƶ�������Q �����������С��C��ȷ���ܶ��ǻ�����������������ݻ��ı�ֵ���ڷ�Ӧ�������������ݻ�ʼ���Dz���ģ�����ѡ��D����ȷ����ѡC��
��B����ȷ�����������ٳ���3.0molM��2.5molN���൱������ѹǿ���ƻ����淴Ӧ�����ƶ�������Q �����������С��C��ȷ���ܶ��ǻ�����������������ݻ��ı�ֵ���ڷ�Ӧ�������������ݻ�ʼ���Dz���ģ�����ѡ��D����ȷ����ѡC��
��ϰ��ϵ�д�
�����Ŀ
 2C(g)����H<0������ʼʱ��M��N�ݻ���ͬ������˵����ȷ���ǣ� ��
2C(g)����H<0������ʼʱ��M��N�ݻ���ͬ������˵����ȷ���ǣ� ��
 2SO3������д���пհף�
2SO3������д���пհף�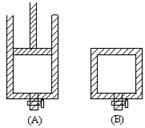
 Z(g) �SH��0����60s�ﵽƽ�⣬����0.3mol Z������˵����ȷ����
Z(g) �SH��0����60s�ﵽƽ�⣬����0.3mol Z������˵����ȷ���� H2��g����CO��g����
H2��g����CO��g���� 2C2 (g)+2D(g)��������Ϊ��Ӧ�ﵽƽ��ı�־��(C )
2C2 (g)+2D(g)��������Ϊ��Ӧ�ﵽƽ��ı�־��(C ) 2C(g) ��H��0
2C(g) ��H��0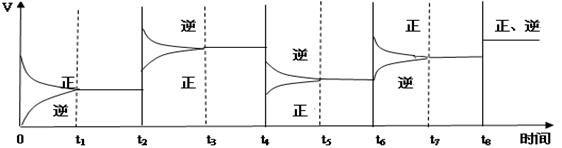
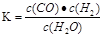
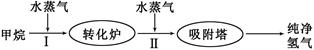
 H2(g)��CO2(g)���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK= ����Ӧ��ƽ�ⳣ�����¶ȵı仯���±���
H2(g)��CO2(g)���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK= ����Ӧ��ƽ�ⳣ�����¶ȵı仯���±���