题目内容
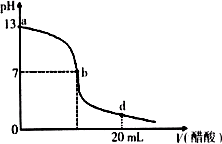
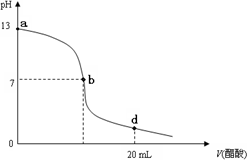
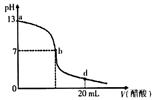
向20 mL氢氧化钠溶液中逐滴加入0.2 mol·L-1醋酸溶液,滴定曲线如下图所示: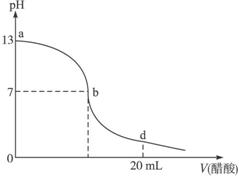
(1)该氢氧化钠溶液的物质的量浓度为___________。
(2)在b点,c(Na+)__________c(CH3COO-)(填“>”“<”或“=”)。
(3)氢氧化钠溶液与醋酸溶液恰好完全反应的点位于曲线的__________(填选项的编号)。
A.a点 B.b点
C.d点 D.a、b间的某点
E.b、d 间的某点
(4)在d点,溶液中所有离子浓度由大到小的顺序为_________________________________。
(1)0.1 mol·L-1 (2)= (3)D
(4)c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
解析:当NaOH与CH3COOH反应呈中性时,CH3COOH稍过量,从图中可以看出,当pH=7时,CH3COOH的体积略大于10 mL,所以可以看出c(NaOH)=![]() c(CH3COOH);在b点,pH=7,c(H+)=c(OH-),所以c(Na+)=c(CH3COO-);当恰好中和时,pH>7,故在a、b点之间;在d点时,溶液酸性很强,pH在2—3附近,离子浓度:c(CH3COO-)>c(Na+)>c(H+)>c(OH-).
c(CH3COOH);在b点,pH=7,c(H+)=c(OH-),所以c(Na+)=c(CH3COO-);当恰好中和时,pH>7,故在a、b点之间;在d点时,溶液酸性很强,pH在2—3附近,离子浓度:c(CH3COO-)>c(Na+)>c(H+)>c(OH-).

|
向20 mL氢氧化钠溶液中逐滴加入0.2 mol/L醋酸溶液,滴定曲线如下图所示下列说法不正确的是
| |
| [ ] | |
A. |
该氢氧化钠溶液的物质的量浓度为0.1 mol/L. |
B. |
在b点,c(Na+)=c(CH3COO-) |
C. |
在d点,溶液中所有离子浓度由大到小的顺序为c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
D. |
氢氧化钠溶液与醋酸溶液恰好完全反应的点位于曲线b、d间的某点 |
向20 mL氢氧化钠溶液中逐滴加入0. 2 mol/L醋酸溶液,滴定曲线如下图所示下列说法不正确的是 ( ) 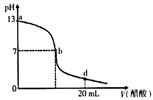
| A.该氢氧化钠溶液的物质的量浓度为0.1 mol/L . |
| B.在b点,c (Na+)=c(CH3COO-) |
| C.在d点,溶液中所有离子浓度由大到小的顺序为 c (CH3COO-)>c (Na+)>c (H+)>c (OH-) |
| D.氢氧化钠溶液与醋酸溶液恰好完全反应的点位于曲线b、d间的某点 |