��Ŀ����
�����ճ���������;��㡢�������Ľ������ϡ�
��1�������£�������������ʢװŨ�����ԭ���� ��
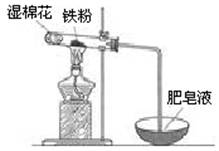
��2��ijʵ��С��������ͼװ����֤����ˮ�����ķ�Ӧ��

��ʪ���������� ���Թ��з�Ӧ�Ļ�ѧ����ʽ�� ��
��ʵ�������ȡ��������Ӧ��Ĺ������Թ��У�����������ᣬ
������ȫ�ܽ⣬������Һ�д��ڵ���������_____ ������ţ���
a��һ����Fe2+��H+��Fe3+ b��һ����Fe2+��H+��������Fe3+
c��һ����Fe2+��Fe3+�������� H+ d��һ����Fe3+��H+��������Fe2+
��3������ȡһ��������������������Ũ�����У����ȣ���ַ�Ӧ���ռ����塣���ⶨ�����к���SO2��CO2��H2��
�� ����Ũ���ᷴӦ�Ļ�ѧ����ʽ�� ��
�� �����л���CO2��ԭ���ǣ��û�ѧ����ʽ��ʾ�� ��
�� ��672 mL����״�����ռ���������ͨ��������ˮ�У���Ӧ�����ӷ���ʽΪ ��Ȼ���������BaCl2��Һ����ϴ�ӡ�����õ�����4.66 g���ɴ���֪�ռ�����������SO2����������� ��
��1�� Ũ����ʹ�������γ�һ�������ȶ�������Ĥ
��2�����ṩˮ����
3Fe+ 4H2O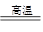 Fe3O4 + 4H2
�� b
Fe3O4 + 4H2
�� b
��3���� 2Fe +
6H2SO4(Ũ)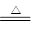 Fe2(SO4)3
+ 3SO2 + 6H2O
Fe2(SO4)3
+ 3SO2 + 6H2O
�� C +2 H2SO4(Ũ)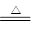 CO2
+2SO2 +2H2O
CO2
+2SO2 +2H2O
�� SO2+Br2+2H2O==2Br- + SO42-+ 4H+ 2/3
����������1�������£�����Ũ�����з����ۻ���Ũ����ʹ�������γ�һ�������ȶ�������Ĥ�����Կ�����������ʢװŨ���ᡣ
��2���ٸ����£�����ˮ������Ӧ��������������ʪ�����������ṩˮ��������Ӧ�ķ���ʽ��3Fe+ 4H2O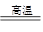 Fe3O4 + 4H2 ��
Fe3O4 + 4H2 ��
�������ڷ�Ӧ�����ǹ����ģ����Է�Ӧ��Ĺ��������У�����������������Ҳ���������������ǹ����ģ�������Һ��һ����Fe2+��H+��������Fe3+����ѡb��
��3����Ũ�������ǿ�����ԣ���������Ũ���ᷴӦ�Ļ�ѧ����ʽ��
2Fe + 6H2SO4(Ũ)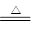 Fe2(SO4)3
+ 3SO2 + 6H2O
Fe2(SO4)3
+ 3SO2 + 6H2O
���������л�ԭ����̼����̼Ҳ�ܺ�Ũ���ᷴӦ������ʽ��C +2 H2SO4(Ũ)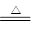 CO2
+2SO2 +2H2O��
CO2
+2SO2 +2H2O��
��SO2�ܰ���ˮ��������Ӧ�ķ���ʽ�� SO2+Br2+2H2O==2Br- + SO42-+ 4H+��4.66g��ɫ���������ᱵ���������ᱵ�����ʵ�����0.02mol����SO2�����ʵ���Ҳ��0.02mol���������0.03mol�����SO2�����������2/3��

 ���������������Բ��������ϵ�д�
���������������Բ��������ϵ�д� �����ճ���������;��㡢�������Ľ������ϣ�
�����ճ���������;��㡢�������Ľ������ϣ�