题目内容
利用所学化学反应原理,解答以下问题:
(1) 某溶液含两种相同物质的量的溶质,其中只存在OH-、H+、NH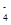 、Cl-四种离子,且c(NH
、Cl-四种离子,且c(NH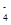 )>c(Cl-)>c(OH-)>c(H+),则这两种溶质是________。
)>c(Cl-)>c(OH-)>c(H+),则这两种溶质是________。
(2) 已知:Ksp(RX)=1.8×10-10,Ksp(RY)=1.5×10-16,Ksp(R2Z)=2.0×10-12,则难溶盐RX、RY和R2Z的饱和溶液中,R+浓度由大到小的顺序是________________________________。
(3) 以石墨电极电解100 mL 0.1 mol·L-1 CuSO4溶液。若阳极上产生气体的物质的量为0.01 mol,则阴极上析出Cu的质量为______g。
(4) 向明矾溶液中逐渐滴加入Ba(OH)2溶液至硫酸根离子刚好沉淀完全时,溶液的pH 7(填“>”、“<”或“=”)离子反应总方程式为_______________________________________,向明矾溶液中逐渐滴加入Ba(OH)2溶液至铝离子刚好沉淀完全时,溶液的pH 7(填“>”、“<”或“=”)离子反应总方程式为 。
(1) 某溶液含两种相同物质的量的溶质,其中只存在OH-、H+、NH
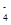 、Cl-四种离子,且c(NH
、Cl-四种离子,且c(NH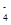 )>c(Cl-)>c(OH-)>c(H+),则这两种溶质是________。
)>c(Cl-)>c(OH-)>c(H+),则这两种溶质是________。(2) 已知:Ksp(RX)=1.8×10-10,Ksp(RY)=1.5×10-16,Ksp(R2Z)=2.0×10-12,则难溶盐RX、RY和R2Z的饱和溶液中,R+浓度由大到小的顺序是________________________________。
(3) 以石墨电极电解100 mL 0.1 mol·L-1 CuSO4溶液。若阳极上产生气体的物质的量为0.01 mol,则阴极上析出Cu的质量为______g。
(4) 向明矾溶液中逐渐滴加入Ba(OH)2溶液至硫酸根离子刚好沉淀完全时,溶液的pH 7(填“>”、“<”或“=”)离子反应总方程式为_______________________________________,向明矾溶液中逐渐滴加入Ba(OH)2溶液至铝离子刚好沉淀完全时,溶液的pH 7(填“>”、“<”或“=”)离子反应总方程式为 。
(共12分)
(1) NH4Cl和NH3·H2O (2分) (2) R2Z>RX>RY(2分) (3) 0.64(2分)
(4) pH>7(1分) Al3++2SO42-+2Ba2++4OH— = AlO2-+2BaSO4↓+2H2O (2分)
pH ="7" (1分) 2Al3++3SO42—+3Ba2++6OH— = 2Al(OH)3↓+3BaSO4↓(2分)
(1) NH4Cl和NH3·H2O (2分) (2) R2Z>RX>RY(2分) (3) 0.64(2分)
(4) pH>7(1分) Al3++2SO42-+2Ba2++4OH— = AlO2-+2BaSO4↓+2H2O (2分)
pH ="7" (1分) 2Al3++3SO42—+3Ba2++6OH— = 2Al(OH)3↓+3BaSO4↓(2分)
试题分析:(1)如溶液为NH4Cl,则溶液中存在c(Cl-)>c(NH4+)>c(H+)>c(OH-),如溶液为NH3·H2O,则溶液中存在
c(NH4+)c(OH-)>c(H+),而c(NH4+)>c(Cl-)>c(OH-)>c(H+),则应为NH4Cl和 NH3·H2O的混合物,
故答案为:NH4Cl和 NH3·H2O。
(2)由Ksp(RX)=1.8×10-10,Ksp(RY)=1.5×10-16,Ksp(R2Z)=2.0×10-12可知,
RX溶液中c(R+)=
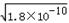 ,RY溶液中c(R+)=
,RY溶液中c(R+)= 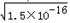 ,R2Z溶液中c(R+)=
,R2Z溶液中c(R+)=  ,
,则R+浓度由大到小的顺序是R2Z>RX>RY,
故答案为:R2Z>RX>RY。
(3)电解CuSO4溶液,阴极反应为:Cu2++2e-=Cu,阳极反应为:2H2O-4e-=4H++O2↑,
当Cu完全析出时,生成n(O2)=(1/2)×0.01mol=0.005mol,而此时在阳极生成0.01mol气体,则标明Cu完全析出,在阴极上还发生:2H++2e-=H2↑,所以生成的铜为m(Cu)=0.01mol×64g/mol=0.64g,
故答案为:0.64。
(4)碱过量,故溶液的pH>7。离子反应总方程式为Al3++2SO42-+2Ba2++4OH— = AlO2-+2BaSO4↓+2H2O。碱反应完,故pH =7,离子反应总方程式为2Al3++3SO42—+3Ba2++6OH— = 2Al(OH)3↓+3BaSO4↓。
点评:本题考查较为综合,涉及弱电解质的电离、盐类的水解、难溶电解质的溶解平衡、电化学以及化学平衡知识,题目难度较大,本题易错点为(6),注意从等效平衡的角度分析。

练习册系列答案
相关题目

 时水的电离平衡曲线应为 (填“A”或“B”)。
时水的电离平衡曲线应为 (填“A”或“B”)。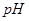 =8的NaOH溶液与
=8的NaOH溶液与 溶液混合,若所得混合溶液的
溶液混合,若所得混合溶液的 的某强酸溶液与1体积
的某强酸溶液与1体积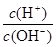 =1×10-8,下列叙述错误的是
=1×10-8,下列叙述错误的是 H++A2- 在0.1mol·L-1Na2A溶液中存在的粒子,其浓度关系正确的是( )
H++A2- 在0.1mol·L-1Na2A溶液中存在的粒子,其浓度关系正确的是( )