题目内容
正确掌握化学用语是学好化学的基础,下列有关表述正确的是( )
①作为相对原子质量测定标准的碳核素:
C
②O2-的结构示意图: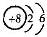
③次氯酸的结构式:Cl-O-H
④CO2的比例(填充)模型:
⑤铝热反应:2Al+3MgO
Al2O3+3Mg
⑥Fe3O4溶于氢碘酸的离子方程式:Fe3O4+8H+
2Fe3++Fe2++4H2O
⑦碳酸氢根离子的水解方程式:HC
+H2O?H3O++C
.
①作为相对原子质量测定标准的碳核素:
14 6 |
②O2-的结构示意图:
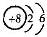
③次氯酸的结构式:Cl-O-H
④CO2的比例(填充)模型:

⑤铝热反应:2Al+3MgO
|
⑥Fe3O4溶于氢碘酸的离子方程式:Fe3O4+8H+
|
⑦碳酸氢根离子的水解方程式:HC
| O | - 3 |
| O | 2- 3 |
| A、③ | B、②③④⑦ |
| C、除①②外 | D、全部 |
分析:①作为相对原子质量测定标准的碳核素为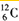 ,不是
,不是
C;
②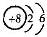 为氧原子结构示意图,不是氧离子的结构示意图;
为氧原子结构示意图,不是氧离子的结构示意图;
③次氯酸中的中心原子为氧原子,分别与氯原子和氢原子形成一个共价键;
④碳原子半径大于氧原子半径,即中间原子应该大于两边的原子;
⑤铝热法是一种利用铝的还原性获得高熔点金属单质的方法;镁比铝活泼,且镁的熔点较低,该反应不会发生;
⑥铁离子具有氧化性,能够氧化碘离子;
⑦碳酸氢根离子水解生成碳酸和氢氧根离子,题中为碳酸氢根离子的电离.
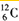 ,不是
,不是14 6 |
②
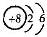 为氧原子结构示意图,不是氧离子的结构示意图;
为氧原子结构示意图,不是氧离子的结构示意图;③次氯酸中的中心原子为氧原子,分别与氯原子和氢原子形成一个共价键;
④碳原子半径大于氧原子半径,即中间原子应该大于两边的原子;
⑤铝热法是一种利用铝的还原性获得高熔点金属单质的方法;镁比铝活泼,且镁的熔点较低,该反应不会发生;
⑥铁离子具有氧化性,能够氧化碘离子;
⑦碳酸氢根离子水解生成碳酸和氢氧根离子,题中为碳酸氢根离子的电离.
解答:解:①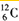 是作为相对原子质量测定标准的碳核素,而不是
是作为相对原子质量测定标准的碳核素,而不是
C,故①错误;
②O2-的核外电子为8,其结构示意图为: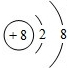 ,故②错误;
,故②错误;
③次氯酸中存在 Cl-O和O-H两个共价键,次氯酸的结构式为:Cl-O-H,故③正确;
④CO2的比例(填充)模型中,碳原子的原子半径大于氧原子, 故④错误;
故④错误;
⑤铝热反应是利用铝的还原性获得高熔点金属单质的方法,镁的活泼性大于铝,但镁的熔点不高,不满足铝热反应的条件,故⑤错误;
⑥将磁性氧化铁溶于氢碘酸,溶液中的碘离子被铁离子氧化成碘单质,溶液中不会存在铁离子,正确的离子方程式为2I-+Fe3O4+8H+=3Fe2++4H2O+I2,故⑥错误;
⑦碳酸氢根离子水解生成碳酸和氢氧根离子,其水解方程式为HCO3-+H2O=H2CO3+OH-,故⑦错误;
故选A.
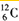 是作为相对原子质量测定标准的碳核素,而不是
是作为相对原子质量测定标准的碳核素,而不是14 6 |
②O2-的核外电子为8,其结构示意图为:
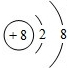 ,故②错误;
,故②错误;③次氯酸中存在 Cl-O和O-H两个共价键,次氯酸的结构式为:Cl-O-H,故③正确;
④CO2的比例(填充)模型中,碳原子的原子半径大于氧原子,
 故④错误;
故④错误;⑤铝热反应是利用铝的还原性获得高熔点金属单质的方法,镁的活泼性大于铝,但镁的熔点不高,不满足铝热反应的条件,故⑤错误;
⑥将磁性氧化铁溶于氢碘酸,溶液中的碘离子被铁离子氧化成碘单质,溶液中不会存在铁离子,正确的离子方程式为2I-+Fe3O4+8H+=3Fe2++4H2O+I2,故⑥错误;
⑦碳酸氢根离子水解生成碳酸和氢氧根离子,其水解方程式为HCO3-+H2O=H2CO3+OH-,故⑦错误;
故选A.
点评:本题考查了常见化学用语的判断,题目难度中等,试题涉及了离子方程式的书写、电子式、比例模型、原子结构示意图等知识,题量稍大,涉及的知识点较多,充分考查了学生对所学知识的掌握情况.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案
相关题目
正确掌握化学用语是学好化学的基础.下列化学用语中正确的是( )
| A、乙烯的结构简式为CH2CH2 | B、葡萄糖的实验式(最简式)为C6H12O6 | C、Ca2+的结构示意图为 | D、NH4Cl的电子式为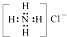 |
正确掌握化学用语是学好化学的基础,下列化学用语正确的是( )
| A、乙烯的结构简式为:CH2CH2 | B、苯的分子式为:C6H6 | C、Cl-的结构示意图为: | D、NaCl的电子式: |
正确掌握化学用语是学好化学的基础.下列化学用语中正确的是( )
| A、乙烯的结构简式为CH2CH2 | B、羟基的电子式: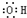 | C、乙醇的分子式:CH3CH2OH | D、乙炔的分子式为C2H2 |