题目内容
粗铜中常含有金、银、铁、锌等杂质,需经过电解精炼.在工业精炼铜的过程中,电解液中C(Cu2+)逐渐下降,C(Fe2+)、C(Zn2+)会逐渐增加.
Ⅰ、写出精炼粗铜过程中阳极上发生的电极反应
Ⅱ、精炼过程中需定时除去其中的Fe2+、Zn2+.下表为部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
甲同学设计了如下除杂方案:
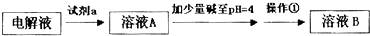
(1)试剂a是
(2)乙同学在查阅资料时发现,“工业原料氯化铵中含杂质氯化铁,使其溶入水,再加入氨水调节pH至7~8,可使Fe3+生成Fe(OH)3沉淀而除去.”乙同学认为甲同学的方案中也应该将溶液pH调至7~8,你认为乙同学的建议是否正确?
Ⅰ、写出精炼粗铜过程中阳极上发生的电极反应
Fe-2e-=Fe2+、Zn-2e-=Zn2+、Cu-2e-=Cu2+
Fe-2e-=Fe2+、Zn-2e-=Zn2+、Cu-2e-=Cu2+
Ⅱ、精炼过程中需定时除去其中的Fe2+、Zn2+.下表为部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
| 开始沉淀 | 2.3 | 7.5 | 5.6 | 6.2 |
| 完全沉淀 | 3.9. | 9.7 | 6.4 | 8.0 |
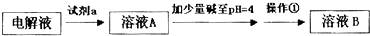
(1)试剂a是
H2O2
H2O2
,其目的是将Fe2+氧化为Fe3+
将Fe2+氧化为Fe3+
;根据上表数据该方案能够除去的杂质金属阳离子是Fe2+
Fe2+
.写出检验该杂质金属阳离子的操作方法:先加入KSCN溶液,若溶液不变红,再滴入几滴氯水,若溶液变成红色,说明含有该离子
先加入KSCN溶液,若溶液不变红,再滴入几滴氯水,若溶液变成红色,说明含有该离子
.(2)乙同学在查阅资料时发现,“工业原料氯化铵中含杂质氯化铁,使其溶入水,再加入氨水调节pH至7~8,可使Fe3+生成Fe(OH)3沉淀而除去.”乙同学认为甲同学的方案中也应该将溶液pH调至7~8,你认为乙同学的建议是否正确?
否
否
(填“是”或“否”),理由是根据沉淀时的pH,当溶液pH为7~8时,溶液A中Cu2+同时生成沉淀而被除去
根据沉淀时的pH,当溶液pH为7~8时,溶液A中Cu2+同时生成沉淀而被除去
.分析:Ⅰ、根据粗铜的组成以及电解池阳极的放电情况来分析;
Ⅱ、(1)电解液中的各种离子沉淀所需要的酸碱性情况不同,可以将亚铁离子氧化为三价铁,根据阳离子以氢氧化物形式沉淀时溶液的pH情况表和亚铁离子以及三价铁的性质来检验;
(2)甲同学的方案中若将溶液pH调至7~8,根据图示表中数据会发现铜离子也会被沉淀.
Ⅱ、(1)电解液中的各种离子沉淀所需要的酸碱性情况不同,可以将亚铁离子氧化为三价铁,根据阳离子以氢氧化物形式沉淀时溶液的pH情况表和亚铁离子以及三价铁的性质来检验;
(2)甲同学的方案中若将溶液pH调至7~8,根据图示表中数据会发现铜离子也会被沉淀.
解答:解:Ⅰ、在粗铜中,含有金属铁、锌、镍金属的活泼性均强于金属铜,所以在阳极上放电的金属是铁、锌、镍、铜,
故答案为:Fe-2e-=Fe2+、Zn-2e-=Zn2+、Ni-2e-=Ni2+、Cu-2e-=Cu2+;
Ⅱ、(1)根据表中数据发现当三价铁离子形成沉淀时,铜离子不沉淀,可以将亚铁离子氧化为三价铁,再调节PH来除去亚铁离子,所以可以选择氧化剂双氧水,向加入双氧水后的溶液中加入KSCN溶液,若溶液不变红,再滴入几滴氯水,若溶液变成红色,说明含有亚铁,故答案为:H2O2;将Fe2+氧化为Fe3+;Fe2+;先加入KSCN溶液,若溶液不变红,再滴入几滴氯水,若溶液变成红色,说明含有该离子;
(2)乙同学的建议不正确,因为根据沉淀时的pH,当溶液pH为7~8时,溶液A中的Cu2+同时会生成沉淀而被除去,故答案为:否;根据沉淀时的pH,当溶液pH为7~8时,溶液A中
Cu2+同时生成沉淀而被除去.
故答案为:Fe-2e-=Fe2+、Zn-2e-=Zn2+、Ni-2e-=Ni2+、Cu-2e-=Cu2+;
Ⅱ、(1)根据表中数据发现当三价铁离子形成沉淀时,铜离子不沉淀,可以将亚铁离子氧化为三价铁,再调节PH来除去亚铁离子,所以可以选择氧化剂双氧水,向加入双氧水后的溶液中加入KSCN溶液,若溶液不变红,再滴入几滴氯水,若溶液变成红色,说明含有亚铁,故答案为:H2O2;将Fe2+氧化为Fe3+;Fe2+;先加入KSCN溶液,若溶液不变红,再滴入几滴氯水,若溶液变成红色,说明含有该离子;
(2)乙同学的建议不正确,因为根据沉淀时的pH,当溶液pH为7~8时,溶液A中的Cu2+同时会生成沉淀而被除去,故答案为:否;根据沉淀时的pH,当溶液pH为7~8时,溶液A中
Cu2+同时生成沉淀而被除去.
点评:本题是一道电化学和化学实验知识相结合的综合题目,难度较大,考查学生分析和解决问题的能力.

练习册系列答案
相关题目