题目内容
通常情况下,CO和O2的混合气体m L用电火花引燃体积变为n L(反应前后条件相同).
(1)试确定混合气体中CO和O2的体积(用V(CO)和V(O2)表示);
(2)若反应后气体的密度在相同条件下为H2密度的15倍,试确定气体成分.
答案:
解析:
解析:
|
(1)由反应方程式2CO+O2 (2)因为 |

练习册系列答案
相关题目
 2CO2可知,反应前后气体体积的变化量等于消耗的O2量,所以消耗的V(O2)=(m-n)L,消耗的V(CO)=2(m-n)L,因为m,n不确定,故分别讨论;若O2不足,则V(O2)=(m-n)L,V(CO)=m-(m-n)=n L;若O2过量,则V(CO)=2(m-n)L,V(O2)=m-2(m-n)=(2n-m)L.
2CO2可知,反应前后气体体积的变化量等于消耗的O2量,所以消耗的V(O2)=(m-n)L,消耗的V(CO)=2(m-n)L,因为m,n不确定,故分别讨论;若O2不足,则V(O2)=(m-n)L,V(CO)=m-(m-n)=n L;若O2过量,则V(CO)=2(m-n)L,V(O2)=m-2(m-n)=(2n-m)L.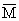 =15×2=30,所以反应后的混合气体中一定有一种式量小于30,故混合气体为CO2与CO.
=15×2=30,所以反应后的混合气体中一定有一种式量小于30,故混合气体为CO2与CO.