题目内容
11.存放食品和药品的包装盒中常可发现一些袋装透明胶状颗粒,该颗粒材料可能的名称及其作用是( )| A. | 活性炭、吸附剂 | B. | KMnO4、氧化剂 | C. | 氯化钠、干燥剂 | D. | 硅胶、干燥剂 |
分析 空气中有水蒸气、氧气,存放食品和药品易和空气中的水蒸气、氧气反应变质,存放食品和药品的包装盒中常可发现一些袋装透明胶状颗粒,该颗粒材料可能除去水蒸气、氧气,据此分析解答.
解答 解:A.活性炭不是透明胶状颗粒,故A错误;
B.KMnO4不是透明胶状颗粒,不是干燥剂,故B错误;
C.氯化钠不具有吸水的特性,不能作为干燥剂使用,也不能吸收氧气,故C错误;
D.硅胶的主要成分为SiO2•nH2O,硅胶具有开放的多孔结构,吸附性强,能吸附多种物质,常用作干燥剂、吸附剂,故D正确;
故选D.
点评 本题考查了硅胶的结构和用途,题目十分简单,平时学习注意基础知识的掌握.

练习册系列答案
相关题目
1.某饱和一元醛和饱和一元酮的混合物共0.1mol,质量为5.8g,此混合物和足量的银氨溶液发生银镜反应可析出8.64g银,则该混合物中的醛是( )
| A. | HCHO | B. | CH3CHO | C. | CH3CH2CHO | D. | CH3CH2CH2CHO |
2.下列物质属于强电解质的是( )
| A. | CH3COOH | B. | BaSO4 | C. | NH3H2O | D. | SO3 |
19.用惰性电极实现电解,下列说法正确的是( )
| A. | 电解稀硫酸溶液,实质上是电解水,故溶液的pH不变 | |
| B. | 电解稀氢氧化钠溶液,要消耗OH-,故溶液的pH减小 | |
| C. | 电解氯化钾溶液,在阴极上和阳极上析出的产物的物质的量之比为1:1 | |
| D. | 电解硫酸钠溶液,在阴极上和阳极上析出的产物的物质的量之比为1:2 |
6.在一定温度下,容积不变的密闭容器里,能说明A(g)+3B(g)?2C(g)达到平衡状态的标志是( )
| A. | 单位时间生成nmol A的同时生成3n mol | |
| B. | B.容器内压强不随时间的变化而变化 | |
| C. | A,B,C的浓度相等的状态 | |
| D. | A,B,C的分子个数比为1:3:2 |
16.水的电离过程为H2O?H++OH-,在不同温度下其平衡常数为:K(25℃)=1.0×10-14 mol2•L-2,K(35℃)=2.1×10-14 mol2•L-2.则下列叙述不正确的是( )
| A. | 纯水的pH随着温度的升高而降低 | B. | 在35℃时,[H+]>[OH-] | ||
| C. | 在25℃和35℃时,[H+]=[OH-] | D. | 水的电离是吸热的 |
20.高纯晶体硅是信息技术的关键材料.
(1)硅元素位于周期表的位置第三周期第ⅣA族.下面有关硅材料的说法中正确的是BCD(填字母).
A.碳化硅化学性质稳定,可用于生产耐高温水泥
B.氮化硅硬度大、熔点高,可用于制作高温陶瓷和轴承
C.高纯度的二氧化硅可用于制造高性能通讯材料---光导纤维
D.普通玻璃是由纯碱、石灰石和石英砂制成的,故在玻璃尖口点燃H2时出现黄色火焰
E.盐酸可以与硅反应,故采用盐酸为抛光液抛光单晶硅
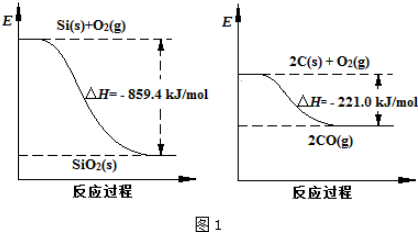
(2)工业上用石英砂和焦炭可制得粗硅.已知:图1
请将以下反应的热化学方程式补充完整:SiO2(s)+2C(s)═Si(s)+2CO(g)△H=+638.4 kJ•mol-1
(3)粗硅经系列反应可生成硅烷(SiH4),硅烷分解生成高纯硅.已知硅烷的分解温度远低于甲烷,用原子结构解释其原因:C和Si最外层电子数相同,C原子半径小于Si,Si元素的非金属性弱于C元素,硅烷的热稳定性弱于甲烷.
(4)将粗硅转化成三氯氢硅(SiHCl3),进一步反应也可制得高纯硅.
①SiHCl3中含有的SiCl4、AsCl3等杂质对晶体硅的质量有影响.根据下表数据,可用蒸馏(或分馏) 方法提纯SiHCl3.
②用SiHCl3制备高纯硅的反应为SiHCl3(g)+H2(g) $\stackrel{一定条件下}{?}$Si(s)+3HCl(g),不同温度下,SiHCl3的平衡转化率随反应物的投料比(反应初始时,各反应物的物质的量之比)的变化关系如图所示.下列说法正确的是ac(填字母序号).
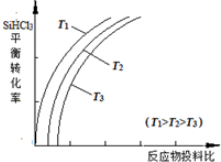
a.该反应的平衡常数随温度升高而增大
b.横坐标表示的投料比应该是$\frac{n(SiHC{l}_{3})}{n({H}_{2})}$
c.实际生产中为提高SiHCl3的利用率,应适当升高温度
③整个制备过程必须严格控制无水无氧.SiHCl3遇水剧烈反应生成H2SiO3、HCl和另一种物质,写出配平的化学反应方程式:SiHCl3+3H2O═H2SiO3↓+H2↑+3HCl↑.

(1)硅元素位于周期表的位置第三周期第ⅣA族.下面有关硅材料的说法中正确的是BCD(填字母).
A.碳化硅化学性质稳定,可用于生产耐高温水泥
B.氮化硅硬度大、熔点高,可用于制作高温陶瓷和轴承
C.高纯度的二氧化硅可用于制造高性能通讯材料---光导纤维
D.普通玻璃是由纯碱、石灰石和石英砂制成的,故在玻璃尖口点燃H2时出现黄色火焰
E.盐酸可以与硅反应,故采用盐酸为抛光液抛光单晶硅
(2)工业上用石英砂和焦炭可制得粗硅.已知:图1
请将以下反应的热化学方程式补充完整:SiO2(s)+2C(s)═Si(s)+2CO(g)△H=+638.4 kJ•mol-1
(3)粗硅经系列反应可生成硅烷(SiH4),硅烷分解生成高纯硅.已知硅烷的分解温度远低于甲烷,用原子结构解释其原因:C和Si最外层电子数相同,C原子半径小于Si,Si元素的非金属性弱于C元素,硅烷的热稳定性弱于甲烷.
(4)将粗硅转化成三氯氢硅(SiHCl3),进一步反应也可制得高纯硅.
①SiHCl3中含有的SiCl4、AsCl3等杂质对晶体硅的质量有影响.根据下表数据,可用蒸馏(或分馏) 方法提纯SiHCl3.
| 物质 | SiHCl3 | SiCl4 | AsCl3 |
| 沸点/℃ | 32.0 | 57.5 | 131.6 |

a.该反应的平衡常数随温度升高而增大
b.横坐标表示的投料比应该是$\frac{n(SiHC{l}_{3})}{n({H}_{2})}$
c.实际生产中为提高SiHCl3的利用率,应适当升高温度
③整个制备过程必须严格控制无水无氧.SiHCl3遇水剧烈反应生成H2SiO3、HCl和另一种物质,写出配平的化学反应方程式:SiHCl3+3H2O═H2SiO3↓+H2↑+3HCl↑.
1.为了探究化学反应中的能量变化,某同学设计了如下两个实验.
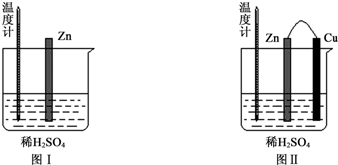
(1)图Ⅰ中发生反应的离子方程式为Zn+2H+═Zn2++H2↑,实验中温度计指示的温度逐渐升高(填“升高”或“降低”),原因是锌与稀硫酸反应是放热反应.
(2)图Ⅱ实验的实验现象如下表,请完成相应实验现象的解释.
(3)若将图中的Cu片替换为Al片,则Al片上的电极反应式为Al-3e-═Al3.

(1)图Ⅰ中发生反应的离子方程式为Zn+2H+═Zn2++H2↑,实验中温度计指示的温度逐渐升高(填“升高”或“降低”),原因是锌与稀硫酸反应是放热反应.
(2)图Ⅱ实验的实验现象如下表,请完成相应实验现象的解释.
| 实验现象 | 解释原因 |
| Cu片上产生了大量气泡 | Zn、Cu构成原电池,H+在Cu片上得电子产生氢气 |
| 温度计指示的温度无明显变化 | 反应中的化学能主要转化成了电能 |