题目内容
中和热测定实验中,下列操作一定会降低实验准确性的是
A 用滴定管(精量仪器,读数保留到0.01)取所用酸碱溶液的体积
B NaOH溶液在倒入小烧杯时,有少量溅出
C、大、小烧杯体积相差较大,夹层间放的碎泡沫塑料较多
D、测量HCl溶液的温度计用水洗净后才用来测NaOH溶液的温度
A 用滴定管(精量仪器,读数保留到0.01)取所用酸碱溶液的体积
B NaOH溶液在倒入小烧杯时,有少量溅出
C、大、小烧杯体积相差较大,夹层间放的碎泡沫塑料较多
D、测量HCl溶液的温度计用水洗净后才用来测NaOH溶液的温度
B
A正确,滴定管的精确高,可准确量取溶液的体积;B错,NaOH溶液在倒入小烧杯时,有少量溅出导致碱的量不足,反应测定出溶液温度变化量减少,即所测中和热的数值将减小;C正确,保温效果越好,实验的准备性越高;D正确,若不洗将,将会损失酸与碱的量,导致所测中和热的值减小,所以,必须洗净后再来测NaOH溶液的温度。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 CH3OH(g)
CH3OH(g) H1
H1 .2mol·L-1,则CO的转化率为 ,此时的温度
.2mol·L-1,则CO的转化率为 ,此时的温度 CH4(g)+3/2O2(g)
CH4(g)+3/2O2(g) l-1。工业上,为选择合适的催化剂,分别对X、Y、Z三种催化剂进行了如下实验(其他条件相同)
l-1。工业上,为选择合适的催化剂,分别对X、Y、Z三种催化剂进行了如下实验(其他条件相同)  T1℃时催化效率最高,能使正反应速率加快约3×105倍;
T1℃时催化效率最高,能使正反应速率加快约3×105倍; CH3OH(g) △H1=-90.7kJ·mol-1
CH3OH(g) △H1=-90.7kJ·mol-1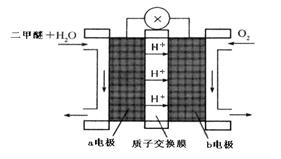
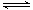 2C(g),在压强相同的条件下,若生成物C的含量w(C)与时间t的关系如图所示。则下列结论正确的是( )
2C(g),在压强相同的条件下,若生成物C的含量w(C)与时间t的关系如图所示。则下列结论正确的是( )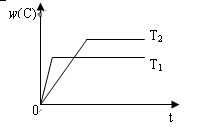
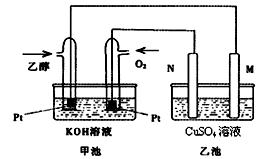
 下),理论上需通入乙醇 g?
下),理论上需通入乙醇 g? 2NH3(g);△H=-92.4kJ·mol-1
2NH3(g);△H=-92.4kJ·mol-1 目前人们处理二氧化碳的方法之一是使其与氢气反应合成甲醇,甲醇是汽车燃料电池的重要燃料。已知氢气、甲醇燃烧的热化学方程式如下:
目前人们处理二氧化碳的方法之一是使其与氢气反应合成甲醇,甲醇是汽车燃料电池的重要燃料。已知氢气、甲醇燃烧的热化学方程式如下: