题目内容
为使溶液中的三种阳离子A+,B2+,C3+逐一沉淀,使之分离,将含有A+,B2+,C3+离子的水溶液进行如图所示实验:

(1)过滤操作用到的仪器用品为________.
(2)B2+________(填“可能”或“不可能”)是Fe2+离子,理由是________.
(3)C3+________(填“可能”或“不可能”)是Fe3+或Al3+,理由是________.
(4)若A+,B2+,C3+分别为Ag+,Cu2+,Al3+,请写出各步反应的离子方程式:________,________,________.
答案:
解析:
解析:
|
(1)分液漏斗、铁圈、铁架台、玻璃棒、滤纸、烧杯;(2)不可能,Fe2+不与H2S反应;(3)可能为Al3+,不可能为Fe3+,因为Fe3+能与H2S反应.而Al3+不与H2S反应,能与NH3·H2O反应;(4)Ag++Cl- 导解:由于FeS可溶于酸,所以Fe2+不能与H2S反应.C3+不可能为Fe3+,因为通入H2S时能将Fe3+反应掉:2Fe3++H2S |

练习册系列答案
 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案
相关题目
为使溶液中的3种阳离子 A+、B2+、C3+逐一沉淀分离,将含有A+、B2+、C3+离子的水溶液进行如下实验,关于三种离子的判断正确的是( )


| A、Ag+、Fe2+、Al3+ | B、NH4+、Fe2+、Fe3+ | C、Ag+、Cu2+、Fe3+ | D、Ag+、Cu2+、Al3+ |
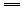 AgCl↓,Cu2++H2S
AgCl↓,Cu2++H2S