题目内容
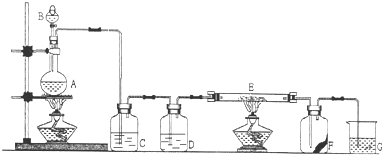
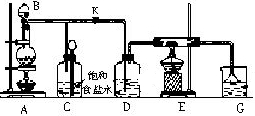
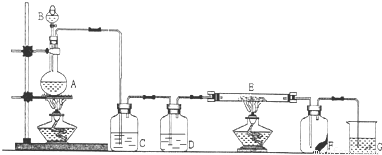
如图是实验室制取氯气并以氯气为原料进行特定反应的装置.其中:A中盛有MnO2,B中盛有浓盐酸.
(1)仪器B的名称
(2)C中盛有饱和食盐水(氯气在其中的溶解度很小),是为了除去氯气中混有的
(3)仪器D用来干燥氯气,其中盛放的试剂是
(4)E中装有铁粉,其中发生的反应的化学方程式是
(5)G中盛有NaOH溶液,目的是

(1)仪器B的名称
分液漏斗
分液漏斗
.(2)C中盛有饱和食盐水(氯气在其中的溶解度很小),是为了除去氯气中混有的
HCl
HCl
气体.(3)仪器D用来干燥氯气,其中盛放的试剂是
浓硫酸
浓硫酸
.(4)E中装有铁粉,其中发生的反应的化学方程式是
2Fe+3Cl2
2FeCl3
| ||
2Fe+3Cl2
2FeCl3
.
| ||
(5)G中盛有NaOH溶液,目的是
吸收多余氯气,防止污染空气
吸收多余氯气,防止污染空气
.其中发生反应的离子方程式是Cl2+2OH-=Cl-+ClO-+H2O
Cl2+2OH-=Cl-+ClO-+H2O
.分析:(1)根据仪器的名称判断;
(2)根据混合气体的成分及杂质的性质分析;
(3)根据杂质气体的性质分析;
(4)根据氯气的性质判断生成物,从而写出方程式;
(5)根据氯气的性质分析,根据离子方程式的书写规则书写.
(2)根据混合气体的成分及杂质的性质分析;
(3)根据杂质气体的性质分析;
(4)根据氯气的性质判断生成物,从而写出方程式;
(5)根据氯气的性质分析,根据离子方程式的书写规则书写.
解答:解:(1)由图可知,仪器B为分液漏斗,答案为:分液漏斗;
(2)浓盐酸有挥发性,所以氯气中含有氯化氢气体,氯化氢极易溶于水,氯气能溶于水,且与水反应,Cl2+H2O=H++Cl-+HClO,食盐水溶液中的氯离子抑制氯气的溶解,降低氯气的溶解度,所以可用饱和食盐水除去氯气中混有的氯化氢气体,故答案为:HCl;
(3)浓硫酸有吸水性,且不和氯气反应,所以可用浓硫酸干燥氯气,故答案为:浓硫酸;
(4)氯气有强氧化性,能把变价金属氧化成最高价态,所以氯气和铁反应的生成物是氯化铁,故答案为:2Fe+3Cl2
2FeCl3;
(5)氯气有毒,污染环境,所以不能排空,氯气能和氢氧化钠反应生成氯化钠、次氯酸钠、水,所以可用氢氧化钠吸收多余的氯气,
故答案为:吸收多余氯气,防止污染空气;Cl2+2OH-=Cl-+ClO-+H2O.
(2)浓盐酸有挥发性,所以氯气中含有氯化氢气体,氯化氢极易溶于水,氯气能溶于水,且与水反应,Cl2+H2O=H++Cl-+HClO,食盐水溶液中的氯离子抑制氯气的溶解,降低氯气的溶解度,所以可用饱和食盐水除去氯气中混有的氯化氢气体,故答案为:HCl;
(3)浓硫酸有吸水性,且不和氯气反应,所以可用浓硫酸干燥氯气,故答案为:浓硫酸;
(4)氯气有强氧化性,能把变价金属氧化成最高价态,所以氯气和铁反应的生成物是氯化铁,故答案为:2Fe+3Cl2
| ||
(5)氯气有毒,污染环境,所以不能排空,氯气能和氢氧化钠反应生成氯化钠、次氯酸钠、水,所以可用氢氧化钠吸收多余的氯气,
故答案为:吸收多余氯气,防止污染空气;Cl2+2OH-=Cl-+ClO-+H2O.
点评:1、氯气有强氧化性,能把变价金属氧化成最高价态;
2、浓盐酸和二氧化锰能反应,稀盐酸和二氧化锰不反应.
2、浓盐酸和二氧化锰能反应,稀盐酸和二氧化锰不反应.

练习册系列答案
相关题目