题目内容
 一定温度和一定体积的条件下反应:A2(s)+2B2(g)?2AB2(g) 达到平衡状态的标志是( )
一定温度和一定体积的条件下反应:A2(s)+2B2(g)?2AB2(g) 达到平衡状态的标志是( )分析:通过化学方程式可知,反应前后气体的化学计量数之和相等,无论是否达到平衡状态,容器的压强都不变,达到平衡状态时,正逆反应速率相等,各物质的浓度不变,由此衍生的一些物理量也不变,以此解答该题.
解答:解:A.反应速率之比应该等于系数比,V正(B2)═V逆(AB2)能说明正逆反应速率相等,故A正确;
B.通过化学方程式可知,反应前后气体的化学计量数之和相等,无论是否达到平衡状态,容器的压强都不变,故B错误;
C.无论该反应是否达到平衡状态,单位时间内生成1molAB2的同时,一定都消耗1mol的B2,故C错误;
D、根据质量守恒,化学反应前后气体混合物的质量变,容器体积不变,所以密度始终变,密度不再随时间变化而变化,证明达到了平衡,故D正确.
故选AD.
B.通过化学方程式可知,反应前后气体的化学计量数之和相等,无论是否达到平衡状态,容器的压强都不变,故B错误;
C.无论该反应是否达到平衡状态,单位时间内生成1molAB2的同时,一定都消耗1mol的B2,故C错误;
D、根据质量守恒,化学反应前后气体混合物的质量变,容器体积不变,所以密度始终变,密度不再随时间变化而变化,证明达到了平衡,故D正确.
故选AD.
点评:本题考查化学平衡状态的判断,题目难度不大,本题易错点为A,注意反应前后气体的化学计量数关系.

练习册系列答案
 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案
相关题目
一定温度和一定体积的条件下反应:A2(s)+2B2(g) 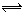 2AB2(g) 达到平衡状态的标志是 ( )
2AB2(g) 达到平衡状态的标志是 ( )
| A.V正(B2)==V逆(AB2) |
| B.容器内的总压强不随时间而变化 |
| C.单位时间内生成1molAB2的同时,消耗1mol的B2 |
| D.气体密度不再随时间变化而变化 |
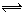 2AB2(g) 达到平衡状态的标志是
( )
2AB2(g) 达到平衡状态的标志是
( ) 2C(g)+D(g);DH<0。现将1 mol A和2 mol B加入甲容器中,将4 mol C和2
mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是
2C(g)+D(g);DH<0。现将1 mol A和2 mol B加入甲容器中,将4 mol C和2
mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是


 CH3OH(g);△H=-90.7 kJ/mol;
CH3OH(g);△H=-90.7 kJ/mol;  CO2(g)+H2(g);△H=-41.2kJ/mol。
CO2(g)+H2(g);△H=-41.2kJ/mol。 CH3OCH3(g) +CO2(g),则该反应的△H=____________
CH3OCH3(g) +CO2(g),则该反应的△H=____________ 
 SiHCl3(l)+ H2(g);
SiHCl3(l)+ H2(g); Si(纯) +3HCl。
Si(纯) +3HCl。