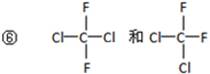
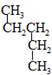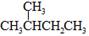题目内容
半透膜与滤纸一样有许多小孔,但孔径比滤纸小,只能通过较小的离子和分子,胶体分散质不能通过半透膜。现把10 mL淀粉胶体和5 mL KCl溶液的混合液体加入用半透膜制成的袋内,将此袋浸入烧杯内的蒸馏水中。2 min后,用两支试管各取5 mL烧杯中的液体,并做如下实验。
(1)向其中一支试管里滴加少量AgNO3溶液,其现象是 。
(2)用另一支试管里的溶液设计实验,证明胶体粒子是否存在? 。
(3)由上述实验得出的结论是 。
(1)出现白色沉淀
(2)向该试管的溶液中滴加少量碘水,无现象(或用一束光照射,溶液中没有产生光亮的通路)
(3)Cl-能透过半透膜,淀粉胶体粒子不能透过半透膜
解析

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案分类法是一种行之有效、简单易行的科学方法。某同学用如表所示的形式对所学知识进行分类,甲与乙、丙、丁是包含关系。其中正确的是
| 选项 | 甲 | 乙、丙、丁 |
| A | 弱电解质 | 一水合氨、水、硫酸钡 |
| B | 腐蚀品 | 浓硫酸、烧碱、硝酸 |
| C | 碱性氧化物 | 过氧化钠、氧化镁、氧化铁 |
| D | 合成高分子材料 | 光导纤维、涤纶、玻璃 |
无机化合物可根据其组成和性质进行分类:
(1)下图所示的物质分类方法名称是________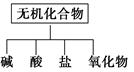
(2)以Na、K、H、O、C、S、N中任两种或三种元素组成合适的物质,分别填在下表②③⑥的后面。
| 物质类别 | 酸 | 碱 | 盐 | 氧化物 |
| 化学式 | HCl②____ | ③___④Ba(OH)2 | ⑤Na2CO3⑥____ | ⑦CO2⑧Na2O2 |
(3)写出⑦转化为⑤的化学方程式_____________________________
(4)呼吸面具中用⑧作为O2来源的反应原理为:___________________________
(5)实验室制备⑦常用________和________反应,检验该气体的方法是____________
(1)下列说法不正确的是________(填字母序号)。
| A.60周年国庆阅兵车HQE顶级红旗采用全铝车身,铝的氧化物属于碱性氧化物 |
| B.用热的纯碱溶液洗涤沾有油污的器具时发生的主要是化学变化 |
| C.英国华裔科学家高锟因在“光在纤维中的传输应用于光学通信方面”做出了突破性成就,而获得了2009年诺贝尔物理学奖,光纤制品的基本原料为SiO2 |
| D.液氨、液氯、液态氯化氢都是非电解质 |
F.化学变化前后原子的种类、数目不变,分子数目也不变
(2)人们对酸碱的认识,已有几百年的历史,经历了一个由浅入深,由低级到高级的认识过程。
①1887年阿仑尼乌斯提出电离理论。
②1923年丹麦化学家布朗斯特和英国化学家劳莱提出了质子论。凡是能够释放质子(氢离子)的任何含氢原子的分子或离子都是酸;凡是能与质子(氢离子)结合的分子或离子都是碱。按质子理论:下列粒子的水溶液既可看作酸又可看作碱的是________(填字母序号)。
AH2O;BNH4+;COH-;DHCO3-;ECH3COO-;FCl-
③1923年路易斯(Lewis)提出了广义的酸碱概念。凡是能给出电子对而用来形成化学键的物质是碱;凡是能和电子对结合的物质都是酸。如
酸(电子对接受体) 碱(电子对给予体) 反应产物
H+ + [OH]- → HOH
试指出下列两个反应中的酸或碱:
H3BO3+H2O=H++[B(OH)4]-
该反应中的碱是________(填“H3BO3”或“H2O”);
CuCl2+4NH3=[Cu(NH3)4]2++2Cl-
该反应中的酸是________(填“CuCl2”或“NH3”)。
胶体是一种重要的分散系。
(1)制备Fe(OH)3胶体是向煮沸的蒸馏水中逐滴加入 溶液,继续煮沸至 ,停止加热。
(2)向Fe(OH)3胶体中加入某种溶液,出现沉淀,继续滴加该溶液后沉淀溶解。滴入的溶液可能是 。
| A.NaOH溶液 | B.稀H2SO4 | C.Na2SO4溶液 | D.乙醇溶液 |
下表是某地市场上销售的一种“加碘盐”包装上的部分文字说明。請根据此表,结合学过的化学知识,回答下列问题:
| 配料表 | 精制海盐、碘酸钾(KIO3) |
| 含碘量 | 20―40mg/kg |
| 储藏方法 | 密封避光、防潮 |
| 食用方法 | 烹调时待食品熟后加入碘盐 |
(2)推测出碘酸钾(KIO3)的物理性质:碘酸钾(KIO3) 溶于水(填“能”或“不能”),化学性质:碘酸钾(KIO3)在受热时 。
能正确表示下列反应的离子方程式是
| A.钠与水反应:Na+2H2O=Na++OH-+H2↑ |
| B.Kl溶液中滴入稀硫酸,空气中振荡:4H+ +41-+O2=2I2+2H2O |
| C.CuCl2溶液中加入氨水:Cu2+ +20H- = Cu(OH)2:↓ |
D.向NH4HCO3溶液中加过量的NaOH溶液并加热:NH4++OH- NH3↑+H2O NH3↑+H2O |
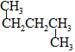 和
和