题目内容
 为了降低某水库的铁闸门被腐蚀的速率,可以采取如图所示的方案,其中焊接在铁闸门上的固体材料R可以采用( )
为了降低某水库的铁闸门被腐蚀的速率,可以采取如图所示的方案,其中焊接在铁闸门上的固体材料R可以采用( )分析:钢铁发生电化学腐蚀时,负极发生氧化反应,正极发生还原反应,防护金属时,可用牺牲阳极的阴极保护法或外加电源的阴极保护法.
解答:解:为了降低某水库的铁闸门被腐蚀的速率,应将铁设计成原电池的正极,则负极为较铁更活泼的金属,
A、金属铜不如金属铁活泼,二者形成的原电池中,金属铜会作正极,故A错误;
B、不可用钠,因钠与水发生剧烈反应,起不到保护铁不被腐蚀的效果,故B错误;
C、金属锌和金属铁构成的原电池中,金属铁作正极,故C正确;
D、金属铁和石墨构成的原电池中,石墨作正极,故D错误;
故选C.
A、金属铜不如金属铁活泼,二者形成的原电池中,金属铜会作正极,故A错误;
B、不可用钠,因钠与水发生剧烈反应,起不到保护铁不被腐蚀的效果,故B错误;
C、金属锌和金属铁构成的原电池中,金属铁作正极,故C正确;
D、金属铁和石墨构成的原电池中,石墨作正极,故D错误;
故选C.
点评:本题考查金属的腐蚀及防护、燃料电池等知识,题目难度中等,注意相关基础知识的积累.

练习册系列答案
相关题目
 AgOH+H+
AgOH+H+
 门上的固体材料R可以采用
门上的固体材料R可以采用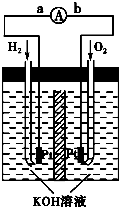 方向为
方向为
