题目内容
一定量的盐酸和过量的铁粉反应,为了减缓反应速率,且不影响生成氢气的量,可向盐酸中加入适量的
| A.KNO3 溶液 | B.K2CO3溶液 | C.CuSO4固体 | D.CH3COONa固体 |
D
试题分析:为了减缓反应速率,且不影响生成氢气的量,所以所加入的物质不能消耗氢离子,所以B错,因为会生成CO2,而A中KNO3 溶液,会形成“氢离子。故选D。
+硝酸根”组合,强氧化性离子组,消耗大量氢离子而生成氮氧化物,所以A错;加入CuSO4固体,会形成铁铜原电池,加快反应速率。C错;加入CH3COONa固体后,氢离子和醋酸根结合会形成弱酸醋酸,使氢离子浓度减小,反应速率减慢,随着反应进行,又会促进醋酸的电离,氢离子又会全部释放,所以不影响生成氢气的量。
点评:该题属于简单的题目,把握反应的本质,就可以解决此类问题

练习册系列答案
相关题目
 3C(g)+4D(g),
3C(g)+4D(g), 2C(g),下列各数据表示不同条件下的反应速率,
2C(g),下列各数据表示不同条件下的反应速率,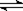 3C(g)+4D(g)的反应,在不同条件下的反应的速率最快的是( )
3C(g)+4D(g)的反应,在不同条件下的反应的速率最快的是( ) 后测得密闭容器内的压强是起始时的0.9倍,在此时间内
后测得密闭容器内的压强是起始时的0.9倍,在此时间内 是
是
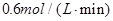


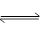 2NH3反应中,自反应开始至2 s末,氨的浓度由0变为0.4 mol·L-1,则以氢气的浓度变化表示该反应在2s内的平均反应速率是( )
2NH3反应中,自反应开始至2 s末,氨的浓度由0变为0.4 mol·L-1,则以氢气的浓度变化表示该反应在2s内的平均反应速率是( )