题目内容
氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为MgCO3,含少量FeCO3)为原料制备高纯氧化镁的实验流程如下: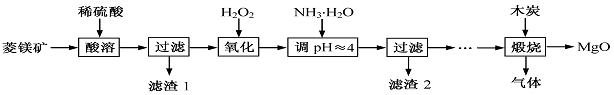 (1)MgCO3与稀硫酸反应的离子方程式为 。
(1)MgCO3与稀硫酸反应的离子方程式为 。
(2)加入H2O2氧化时,发生反应的化学方程式为 。(3)滤渣2的成分是 (填化学式)。
(4)煅烧过程存在以下反应:2MgSO4+C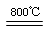 2MgO+2SO2↑+CO2↑、MgSO4+C
2MgO+2SO2↑+CO2↑、MgSO4+C MgO+SO2↑+CO↑、 MgSO4+3C
MgO+SO2↑+CO↑、 MgSO4+3C MgO+S↑+3CO↑。
MgO+S↑+3CO↑。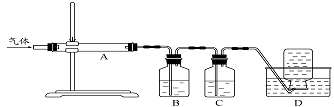
利用上图装置对煅烧产生的气体进行分步吸收或收集。
①D中收集的气体是 (填化学式)。
②B中盛放的溶液可以是 (填字母)。
a.NaOH 溶液 b.Na2CO3溶液 c.稀硝酸 d.KMnO4溶液
③A中得到的淡黄色固体与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式: 。
(11分)(1)MgCO3+2H+=Mg2++CO2↑+H2O(2分)
(2)2FeSO4+H2O2+H2SO4=Fe2(SO4)3+2H2O (2分) (3)Fe(OH)3(2分)
(4) ① CO(1分) ②d (2分) ③3S+6OH- 2S2-+SO32-+3H2O(2分,不写条件扣1分)
2S2-+SO32-+3H2O(2分,不写条件扣1分)
解析试题分析:(1)MgCO3与稀硫酸发生复分解反应生成硫酸镁、二氧化碳和水,反应的离子方程式为MgCO3+2H+=Mg2++CO2↑+H2O。
(2)由于滤液中含有亚铁离子,需要氧化成铁离子通过控制pH形成氢氧化铁沉淀而除去,所以加入H2O2的目的是在在酸性溶液中氧化硫酸亚铁为硫酸铁,反应的化学方程式为2FeSO4+H2O2+H2SO4=Fe2(SO4)3+2H2O。
(3)酸溶后过滤得到溶液中加入过氧化氢氧化亚铁离子为铁离子,加入氨水调节溶液pH使铁离子全部生成氢氧化铁沉淀,所以过滤后得到沉淀为氢氧化铁,即滤渣2的主要成分是氢氧化铁。
(4)①根据煅烧时发生反应的方程式可知,煅烧得到的气体主要有SO2、CO2、CO、S,产生的气体进行分步吸收或收集,所以通过A使硫蒸气冷凝下来。最后剩余的气体可以用排水法收集,这说明该气体应该是CO。
②由于吸收CO2一般用碱液,而SO2也能被碱液吸收,所以首先吸收SO2,即通过B装置吸收SO2。可以利用SO2的还原性,将SO2通入到高锰酸钾溶液吸收中二氧化硫,再通过C装置中的氢氧化钠溶液吸收二氧化碳。
③A中得到的淡黄色固体与热的NaOH溶液反应,依据氧化还原反应原理,产物中元素最高价态为+4,则该生成物应该是亚硫酸钠。S元素的最低价为-2价,即还原产物是氯化钠,因此反应的离子方程式为3S+6OH- 2S2-+SO32-+3H2O。
2S2-+SO32-+3H2O。
考点:考查工艺流程题的判断、混合物的分离、方程式书写等

(14分)某研究性学习小组在网上收集到如下信息:硫化钠,俗称臭碱,是一种强还原剂,在工业上用途广泛。他们对硫化钠与次氯酸钠的反应进行探究。
【实验】
在次氯酸钠溶液中加入硫化钠溶液,发现溶液始终澄清。
(1)下列有关硫化钠的说法正确的是 。
a. 硫化钠溶液不宜久置,应现用现配
b. 硫化钠溶液中通入SO2有淡黄色浑浊,可证明SO2有氧化性
c. 硫化钠在空气中潮解并不断放出H2S气体,说明酸性:H2CO3>H2S
d. 配制硫化钠溶液时加入少量氢氧化钾
e. 向硫化钠溶液中滴加稀硝酸有臭鸡蛋气味的气体生成
【提出假设】
(2)反应后的溶液中肯定存在Cl-、SO42-和OH-,为探究溶液中可能还存在的其他阴离子(不考虑离子水解及空气中CO2的影响),该学习小组提出如下假设:
假设1:只还存在S2-
假设2:只还存在ClO-
假设3:
【设计实验方案,验证假设】
(3)请写出实验步骤以及预期现象和结论。
限选实验试剂:1 mol? L-1的CuSO4溶液、1 mol? L-1NaOH溶液、淀粉-KI溶液、紫色石蕊试液、酚酞试液。
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少许反应后溶液于试管中,滴加 | 若 ,则假设 成立。 |
| 步骤:2:另取少许反应后溶液于试管中,滴加 | 若 ,则假设 成立。 若 , 则假设3成立。 |
【思考与交流】
(4)实验时某同学发现所用硫化钠溶液呈黄色,联想到工业盐酸呈黄色的原因,该同学认为所用硫化钠溶液中混有少量FeCl3。你是否同意该同学的的观点 (填“同意”或“不同意”),请简述理由: 。
化学实验研究的常用方法,
| A.蒸馏 | B.萃取 | C.过滤 | D.结晶 E.分液 F.纸上层析,请填空(填字母): |
用四氯化碳提取溴水中的溴单质的方法 ;
分离乙酸(沸点118℃)与乙酸乙酯(沸点77.1℃)的方法 ;
从含有少量氯化钠的硝酸钾溶液中提取硝酸钾的方法 。
海洋植物如海带、海藻中含有丰富的碘元素,其主要以碘化物形式存在。有一化学课外小组用海带为原料制取少量碘单质,他们将海带灼烧成灰,用水浸泡一段时间(以让碘化物充分溶解在水中),得到海带灰悬浊液,然后按以下实验流程提取单质碘:
(1)指出提取碘的过程中有关的实验操作名称:① ,③ ;
(2)操作③中所用的有机试剂可以是 (只填一种),简述选择其理由 。
(3)操作过程③可以分解为如下几步:
| A.把盛有溶液的分液漏斗放在铁架台的铁圈中; |
| B.把50ml碘水和15ml有机溶剂(你所选的)加入分液漏斗中,并盖好玻璃塞; |
| C.检验分液漏斗活塞和上口的玻璃塞是否漏液; |
| D.倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正; |
F.从分液漏斗上口倒出上层液体;
G.将漏斗上口的玻璃塞打开或使塞上的凹槽与漏斗上口的小孔对准;
H.静置、分层。
(a)过程③正确操作步骤的顺序是:(填编号字母) ;
(b)上述G步操作的目的是: ;

 BaS(s)+4CO2(g),该反应的平衡常数的表达式为__________________________________________________。
BaS(s)+4CO2(g),该反应的平衡常数的表达式为__________________________________________________。
 MgCl2 + 6H2O,该反应要在HCl气流中进行,原因是 。
MgCl2 + 6H2O,该反应要在HCl气流中进行,原因是 。


 、
、 、
、 、
、 等]。某主要生产
等]。某主要生产 、
、 的化工厂利用钡泥制取
的化工厂利用钡泥制取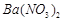 ,其部分工艺流程如下:
,其部分工艺流程如下:
 ,
, 的反应化学方程式为 。
的反应化学方程式为 。