题目内容
将含O2和CH4的混合气体充入装有23.4gNa2O2的密闭容器中点燃,反应结束后,容器温度为150℃,压强为0pa,将残留物溶于水无气体逸出。下列叙述正确的是( )
| A.原混合气体中O2和CH4的体积比为2:1 |
| B.原混合气体中O2和CH4的体积比为1:3 |
| C.残留固体中有Na2CO3和NaOH |
| D.残留固体中只有Na2CO3 |
C
依题意反应后容器温度为150℃,压强为0pa,知产物无气体和水。依据原子守恒推断产物应为Na2CO3和NaOH,配平如下:O2+ 2CH4+6Na2O2= 2Na2CO3+8NaOH(先根据碳原子和氢原子守恒配平),由方程式可知A、B、D均错误,故选C。

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目
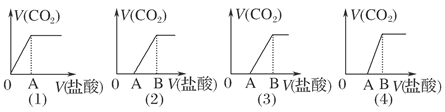
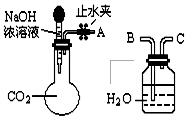
 假设2:该固体只有Na2CO3;
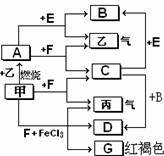
假设2:该固体只有Na2CO3;  18号元素组成的一些单质及其化合物之间的转化关系图。常温常压下,D、F、K均为无色无刺激性气味的气体,B是最常见的无色液体,A是由单质C在D中燃烧生成的淡黄色固体。(反应中生成的部分物质已略去)
18号元素组成的一些单质及其化合物之间的转化关系图。常温常压下,D、F、K均为无色无刺激性气味的气体,B是最常见的无色液体,A是由单质C在D中燃烧生成的淡黄色固体。(反应中生成的部分物质已略去)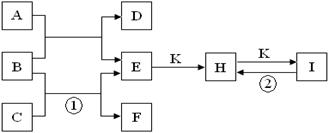
 在电火花点火的情况下,两者恰好完全反应后恢复到原温度时,容器为真空且碳元素全部以正盐的形式存在,则CH4,O2,Na2O2的物质的量之比为 。
在电火花点火的情况下,两者恰好完全反应后恢复到原温度时,容器为真空且碳元素全部以正盐的形式存在,则CH4,O2,Na2O2的物质的量之比为 。