题目内容
1.B、C、D、E、F是原子序数依次增大的短周期主族元素,B是短周期中金属性最强的元素,C是同周期中离子半径最小的元素,D元素的最高价氧化物对应水化物与B元素的最高价氧化物对应水化物反应的产物M是制备木材防火剂的原料,E的最外层电子数与内层电子数之比为3﹕5.请回答:(1)D的原子结构示意图为
 .
.(2)写出工业制F单质的化学方程式:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑.
(3)用电子式表示元素B与元素F形成的化合物:
 .
.(4)B单质与氧气反应的产物与C的单质同时放入水中,产生两种无色气体,有关的化学方程式为2Na2O2+2H2O═4NaOH+O2↑、、2Al+2NaOH+2H2O═2NaAlO2+3H2↑.
(5)写出M与盐酸反应的离子方程式:SiO3 2-+2H+=H2SiO3↓.
(6)工业上将干燥的F单质通入熔融的E单质中可制得化合物E2F2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,该反应的化学方程式为2S2Cl2+2H2O═3S↓+SO2↑+4HCl.
分析 B是短周期中金属性最强的元素,则B为Na;而B、C、D、E、F是原子序数依次增大的短周期主族元素,元素均处于第三周期,C是同周期中离子半径最小的元素,则C为Al;D元素的最高价氧化物对应水化物与B元素的最高价氧化物对应水化物反应的产物M是制备木材防火剂的原料,则D为Si,M为Na2SiO3,E的最外层电子数与内层电子数之比为3﹕5,则最外层电子数为6,故E为S元素,则F为Cl元素,据此解答.
解答 解:B是短周期中金属性最强的元素,则B为Na;而B、C、D、E、F是原子序数依次增大的短周期主族元素,元素均处于第三周期,C是同周期中离子半径最小的元素,则C为Al;D元素的最高价氧化物对应水化物与B元素的最高价氧化物对应水化物反应的产物M是制备木材防火剂的原料,则D为Si,M为Na2SiO3,E的最外层电子数与内层电子数之比为3﹕5,则最外层电子数为6,故E为S元素,则F为Cl元素.
(1)D为Si元素,原子结构示意图为: ,故答案为:
,故答案为: ;
;
(2)工业制氯气的化学方程式:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑,故答案为:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑;
(3)元素B与元素F形成的化合物为NaCl,其电子式为: ,故答案为:
,故答案为: ;
;
(4)Na与氧气反应的产物与Al单质同时放入水中,产生两种无色气体,应是过氧化钠与水反应生成氢氧化钠与氧气,氢氧化钠与Al反应生成偏铝酸钠与氢气,有关的化学方程式为:2Na2O2+2H2O═4NaOH+O2↑、2Al+2NaOH+2H2O═2NaAlO2+3H2↑,
故答案为:2Na2O2+2H2O═4NaOH+O2↑、2Al+2NaOH+2H2O═2NaAlO2+3H2↑;
(5)Na2SiO3与盐酸反应的离子方程式:SiO3 2-+2H+=H2SiO3↓,
故答案为:SiO32-+2H+=H2SiO3↓;
(6)工化合物S2Cl2可与水反应生成一种能使品红溶液褪色的气体,该气体为SO2,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,故S元素化合价降低,转移0.3mol电子生成二氧化硫为0.1mol,故有0.3molS原子发生还原反应,根据电子转移守恒可知S元素在还原产物中的化合价为0,故生成S,同时生成HCl,该反应的化学方程式为:2S2Cl2+2H2O═3S↓+SO2↑+4HCl,
故答案为:2S2Cl2+2H2O═3S↓+SO2↑+4HCl.
点评 本题考查结构性质位置关系应用,推断元素是解题关键,侧重对化学用语的考查,考查学生运用知识分析问题、解决问题的能力,难度中等.

| A | 最外层电子数是电子层数的2倍,单质为黑色固体 |
| B | 单质是空气的主要成分之一 |
| C | 与B不同主族,单质为淡黄色固体,易溶于二硫化碳 |
| D | 一种非金属元素 |
| E | 与D形成的某种化合物的水溶液遇苯酚溶液显紫色 |
(2)元素A和B中非金属性更强的元素是(填名称):氮,支持此结论的一种实验事实为硝酸的酸性比碳酸的酸性强
(3)元素C和D可以形成共价化合物C2D2,该化合物中各原子都达到8电子稳定结构,则该化合物的电子式为
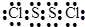
(4)已知液态CS2完全燃烧生成两种同价态的气体氧化物,若生成的两种气体总体积为3360mL(已折算为标准状况)时,反应放出Q (Q>0)kJ的热量,则表示CS2燃烧热的热化学方程式为CS2(l)+3O2(g)=CO2(g)+2SO2(g)△H=-20QkJ•mol-1
(5)向B的气态氢化物水溶液中,通入A的最高价氧化物,可能得到两种盐:X和Y.同温下等浓度的X和Y的溶液中,pH更高的是(填名称)碳酸铵
(6)元素D和E形成的不与苯酚溶液显色的化合物为F,则检验F溶液中阳离子的方法为取少量溶液于试管中,滴加铁氰化钾溶液出蓝色沉淀,向F的溶液中加入过氧化钠可以得到红褐色沉淀,同时没有气体产生,则该反应过程中离子反应方程式为6Fe2++3Na2O2+6H2O=4Fe(OH)3↓+6Na++2Fe3+(用一个总的离子方程式表示)
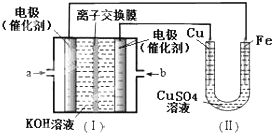
| A. | a处通入O2 | B. | b处发生氧化反应 | ||
| C. | 电流由Cu电极移向b | D. | Fe电极发生的反应为:Cu2++2e-=Cu |
| A. | 血糖过低的患者可利用静脉注射葡萄糖溶液的方法迅速补充营养 | |
| B. | 装运乙醇的包装箱应贴的图标是 | |
| C. | 用活性炭为糖浆脱色和用SO2漂白纸浆的原理不同 | |
| D. | 海水淡化的方法有蒸馏法、电渗析法等 |
| A. | 合成高效、稳定、廉价的太阳能光电转化材料,是开发利用太阳能的关键 | |
| B. | 大量焚烧田间秸秆会产生雾霾,“雾”和“霾”的分散质微粒不同 | |
| C. | 肥皂能去污的原理,是其在水溶液中能电离出钠离子(亲水基团)和硬脂酸根离子(亲油基团),在它们的共同作用下,通过搓洗,将衣服上的油污“拖下水” | |
| D. | 我国已能利用3D打印技术,以钛合金粉末为原料,通过激光熔化逐层堆积,来制造飞机钛合金结构件,高温时可用金属钠还原相应的氯化物来制取金属钛 |
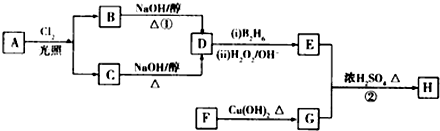
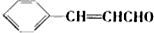 回答下列问题:
回答下列问题: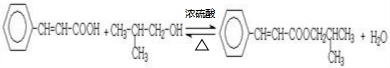 .
.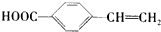 .
.

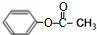 .
.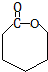 .
. .
. .
. .
. .
.