题目内容
向Cu、Cu2O和CuO组成的混合物中,加入1 L 0.6 mol·L -1HNO3溶液恰好使混合物溶解,同时收集到2240 mL NO气体(标准状况)。(已知:Cu2O+2H+=Cu+Cu2++H2O)
(1)Cu2O跟稀硝酸反应的离子方程式 。
(2)若将上述混合物用足量的H2加热还原,所得到固体的质量为 g。
(3)若混合物中含0.1 mol Cu,将该混合物与稀硫酸充分反应,至少消耗H2SO4的物
质的量为 。
(1)3Cu2O+ 14H+ + 2NO3-=6Cu2+ +2 NO↑+ 7H2O (2)16 (3)0.1mol
【解析】
试题分析:(1)Cu2O跟稀硝酸反应的离子方程式为3Cu2O+ 14H+ + 2NO3-=6Cu2+ +2 NO↑+ 7H2O 。(2)n(HNO3)=0.6mol,n(NO)=2.24L÷22.4L/mol=0.1mol.所以n(Cu(NO3)2)=1/2n(NO3-)=0.25mol.所以若将上述混合物用足量的H2加热还原,所得到固体的质量即为Cu的质量。m(Cu)= 0.25mol×64g/mol=16g。(3)若混合物中含0.1 mol Cu,根据方程式3Cu+8HNO3(稀)=2Cu(NO3)2+2NO↑+4H2O可知Cu产生的NO的物质的量为0.2/3mol,则Cu2O与硝酸反应产生的NO的物质的量为0.1mol-2/3×0.1mol=0.1/3mol. 在根据3Cu2O+ 14H+ + 2NO3-=6Cu2+ +2 NO↑+ 7H2O 可计算出Cu2O的物质的量为0.0 5mol.所以CuO物质的量为(0.15-0.2/3-0.1/3)mol=0.05mol结合方程式: CuO+H2SO4=CuSO4+H2O; Cu2O+H2SO4=Cu+ Cu SO4+H2O.可知:消耗的H2SO4的物质的量为0.05mol+0.05mol=0.1mol.
考点:考查Cu、Cu2O和CuO与硝酸、硫酸反应原理及离子方程式的书写及个组分含量的计算。


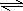 Cu(OH)2+2H+
Cu(OH)2+2H+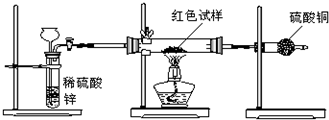
 2Cu+SO2反应制取粗铜,当有32gCu2S消耗时,电子转移数目是
。
2Cu+SO2反应制取粗铜,当有32gCu2S消耗时,电子转移数目是
。