题目内容
下列叙述中正确的是( )A.离子化合物中不可能存在非极性键
B.非极性分子中不可能既含极性键又含非极性键
C.非极性分子中一定含有非极性键
D.不同非金属元素原子之间形成的化学键都是极性键
解析:判断“不可能存在”“一定含有”“都是”等类结论的正误时,一般可用反例法。即只要能举出一个可以成立的反例来,则可否定题中结论,如果不存在反例,则可认为题中结论正确。
A项离子化合物中可能存在非极性键。如Na2O2是离子化合物,其中O—O键是非极性键,故A错误。
B项非极性分子中,既含非极性键又含极性键是可能的。如乙炔(H—C≡C—H)分子中,C—H键是极性键,C≡C键是非极性键。
C项由极性键组成的多原子分子,只要分子结构对称就是非极性分子。如CO2(O=C=O)是非极性分子,分子中所有化学键都是极性键,故C也是错误的。
D项叙述正确。因为不同非金属原子吸引电子的能力不同,它们之间的共用电子对必偏向其中一方而形成极性共价键。
答案:D

练习册系列答案
相关题目
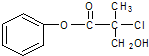 有机物A是农药生产中的一种中间体,结构简式如图所示.下列叙述中正确的是( )
有机物A是农药生产中的一种中间体,结构简式如图所示.下列叙述中正确的是( )| A、有机物A可以在一定条件下与HBr发生反应 | B、1mol A最多能与4mol H2发生加成反应 | C、有机物A与浓硫酸混合加热,可以发生消去反应 | D、1mol A与足量的NaOH溶液反应,最多可以消耗3mol NaOH |


