��Ŀ����
��ͬ�¶��£��ݻ���ͬ�ļס������������ܱ������о��������·�Ӧ��2SO2(g) + O2(g)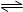 2SO3(g) + 197 kJʵ�����й��������£�
2SO3(g) + 197 kJʵ�����й��������£�
�����ж��в���ȷ����
A��197��Q1��Q2
B���ﵽƽ��ʱSO2������������ף���
C���������з�Ӧ��ƽ�ⳣ�����
D������1molSO3(l)ʱ�ų�����������98.5kJ
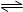 2SO3(g) + 197 kJʵ�����й��������£�
2SO3(g) + 197 kJʵ�����й��������£�| ������� | ��ʼʱ�����ʵ����ʵ��� / mol | �ﵽƽ��ʱ��ϵ�����ı仯/KJ | ||
| SO2 | O2 | SO3 | ||
| �� | 2 | 1 | 0 | �ų�������Q1 |
| �� | 1.8 | 0.9 | 0.2 | �ų�������Q2 |
�����ж��в���ȷ����
A��197��Q1��Q2
B���ﵽƽ��ʱSO2������������ף���
C���������з�Ӧ��ƽ�ⳣ�����
D������1molSO3(l)ʱ�ų�����������98.5kJ
B
���������A�м���������Ӧ������ƽ�⣬�����ǿ��淴Ӧ������ȫת������197��Q1������ƽ���Ǵ�������������н����ģ��ų�������Ȼ����Q1��Q2��A��ȷ��B�������ǵ�Чƽ��ﵽƽ��ʱSO2�����������=�ң��������¶ȱ仯������ƽ�ⳣ��ֻ���¶��йأ��¶���ͬ��Ȼ��ȣ���ȷ�� D��������1molSO3(g)ʱ�ų�������������98.5kJ��������̬��Һ̬ʱ��Ҫ�ų�������������1molSO3(l)ʱ�ų�����������98.5kJ����ȷ��

��ϰ��ϵ�д�
�����Ŀ
 H++Cl-+HClO������˵������ȷ����(����)
H++Cl-+HClO������˵������ȷ����(����)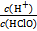 ����
���� 2NO2(g)����H����57 kJ��mol��1�����¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯������ͼ��ʾ������˵����ȷ����( )
2NO2(g)����H����57 kJ��mol��1�����¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯������ͼ��ʾ������˵����ȷ����( )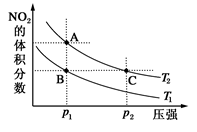
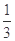 Fe2O3��s��+ CO��g��
Fe2O3��s��+ CO��g�� 
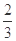 Fe��s��+CO2��g��+Q
Fe��s��+CO2��g��+Q xC(g) ��H��0�����������c(A)��ʱ��t�ı仯��ͼ��ʾ��
xC(g) ��H��0�����������c(A)��ʱ��t�ı仯��ͼ��ʾ��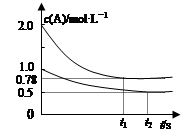
 2NH3(g)������ʼʱֻ����2a mol NH3���ﵽƽ��ʱ����������ѹǿ����ʼʱ������40%����ͬ�����¿�ʼʱ����a mo N2��3a mol H2�Ļ�����壬��
2NH3(g)������ʼʱֻ����2a mol NH3���ﵽƽ��ʱ����������ѹǿ����ʼʱ������40%����ͬ�����¿�ʼʱ����a mo N2��3a mol H2�Ļ�����壬�� 2NH3(g)������ʼʱֻ����2a mol NH3���ﵽƽ��ʱ����������ѹǿ����ʼʱ������40%������ʼʱ����a mo N2��3a mol H2�Ļ�����壬��
2NH3(g)������ʼʱֻ����2a mol NH3���ﵽƽ��ʱ����������ѹǿ����ʼʱ������40%������ʼʱ����a mo N2��3a mol H2�Ļ�����壬�� 2NH3������ƽ����ϵ�и����ʵ�Ũ�ȶ����ӵ�ԭ����2����������Ľ����
2NH3������ƽ����ϵ�и����ʵ�Ũ�ȶ����ӵ�ԭ����2����������Ľ����