题目内容
1.随着社会的发展,人们日益重视环境问题,下列说法不正确的是( )| A. | 绿色化学的核心是利用化学原理从源头上减少和消除化学工业生产对环境的污染 | |
| B. | 对废旧电池进行回收处理主要是为了防止重金属污染水源和土壤 | |
| C. | 采用催化转换技术将汽车尾气中的NOx和CO转化为无毒气体 | |
| D. | PM2.5是指大气中直径接近于2.5×10-6m的细颗粒物,它们分散在空气中形成的混合物具有丁达尔效应 |
分析 A.绿色化学的核心是从源头上减少或消除对环境的影响;
B.废旧电池中含有重金属,重金属能污染水源和土壤;
C.汽车尾气中的NOx和CO在催化作用下可生成氮气和二氧化碳;
D.如粒子直径大于100nm,则不能产生丁达尔效应;
解答 解:A.绿色化学的核心是利用化学原理从源头上减少和消除工农业生产等对环境的污染,不是先造成环境污染,然后再处理,故A正确;
B.废旧电池中含有重金属,重金属能污染水源和土壤,所以对废旧电池进行回收处理,故B正确;
C.汽车尾气中的NOx和CO在催化作用下可生成氮气和二氧化碳,故C正确;
D.PM2.5不一定形成胶体,如粒子直径大于100nm,则不能产生丁达尔效应,故D错误;
选故:D.
点评 本题主要考查环境污染与防治等知识点,侧重于基础知识的考查,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.Fe和Fe2O3 的混合物共13.6g,加入150mL稀H2SO4,在标准状况下收集到1.12LH2,Fe和Fe2O3 均无剩余.为中和过量的H2SO4,并使Fe元素全部转化为Fe(OH)2 沉淀,消耗了200mL 3mol/L的NaOH溶液,则该H2SO4 的物质的量浓度为( )
| A. | 2.25mol/L | B. | 2mol/L | C. | 4mol/L | D. | 0.6mol/L |
9.下列说法不正确的是( )
| A. | 将pH均为a的氢氧化钠溶液和氨水分别加水稀释100倍,pH变为b和c,则a、b、c的大小关系是:a>c>b | |
| B. | 常温下,浓度均为0.1mol/L ①醋酸、②盐酸、③醋酸钠溶液,水的电离程度由大到小的顺序为:③>①>② | |
| C. | 物质的浓度相同的:①氯化铵溶液、②硫酸铵溶液、③碳酸氢铵溶液,pH由大到小的顺序为:③>①>② | |
| D. | 常温下,将相同体积的pH=3硫酸和pH=11一元碱BOH溶液混合,所得溶液可能为中性也可能为酸性 |
16.锌粉、铝粉的混合物44g与一定量浓度为17.25%的硫酸溶液恰好反应,将溶液蒸发结晶得干燥的无水固体140g,则放出的气体在标准状况下的体积为( )
| A. | 无法计算 | B. | 6.72L | C. | 33.6L | D. | 22.4L |
13.对于等物质的量浓度的Na2CO3和NaHCO3溶液,下列说法错误的是( )
| A. | 相同温度下两种溶液的pH:Na2CO3>NaHCO3 | |
| B. | 若分别升高温度,两种溶液的pH均减小 | |
| C. | 若分别加入少量NaOH,两溶液中c(CO32-)均增大 | |
| D. | 两溶液中的离子浓度均存在关系:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-) |
10.下列有关物质的性质和该性质的应用均正确的是( )
| A. | 二氧化硅不与任何酸反应,可用石英制造耐酸容器 | |
| B. | 二氧化氯具有还原性,可用于自来水的杀菌消毒 | |
| C. | 常温下浓硫酸使铝钝化,可在常温下用铝制贮罐贮运浓硫酸 | |
| D. | 二氧化氮溶于水时只生成唯一产物硝酸,工业上利用这一原理生产硝酸 |
11.从碘的有机溶液中回收有机溶剂,可选用的实验装置是( )
| A. | 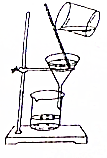 | B. | 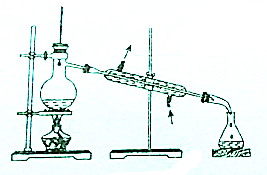 | ||
| C. | 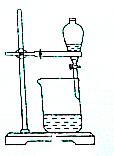 | D. | 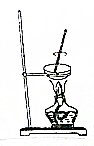 |
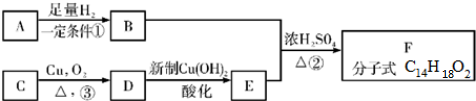
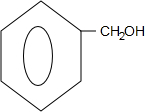 .
.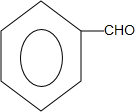 +2H2O;
+2H2O; +
+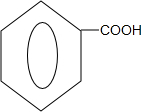 $?_{△}^{浓硫酸}$
$?_{△}^{浓硫酸}$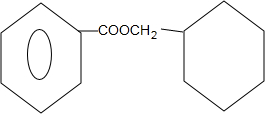 +H2O.
+H2O. .
.